题目内容
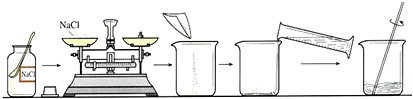
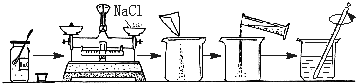
10.海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程如图:
请回答下列问题:
(1)A的化学式是CaO;B的化学式是Ca(OH)2.
(2)写出步骤②发生反应的化学方式CaO+H2O═Ca(OH)2.
(3)写出步骤③发生反应的化学方式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 (1)贝壳的主要成分为CaCO3,碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,进行分析解答.
(2)步骤②,即氧化钙与水反应生成氢氧化钙,写出反应的化学方程式即可.
(3)步骤③,即氢氧化钙与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,写出反应的化学方程式即可.
解答 解:(1)贝壳的主要成分为CaCO3,碳酸钙高温分解生成氧化钙和二氧化碳,氧化钙与水反应生成氢氧化钙,则A为氧化钙,B为氢氧化钙,其化学式分别是CaO、Ca(OH)2.
(2)步骤②,即氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.
(3)步骤③,即氢氧化钙与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:(1)CaO;Ca(OH)2;(2)CaO+H2O═Ca(OH)2;(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题难度不大,熟练掌握碳酸钙、氧化钙、氢氧化钙之间的转化、盐的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
相关题目
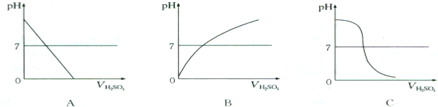
15.某同学进行中和反应实验:取适量的NaOH溶液于烧杯中,滴加几滴紫色石蕊试液,再逐渐滴加稀H2SO4,测得溶液的pH及颜色变化情况如表:
(1)如图中符合上述实验过程的图形是C
(2)当加入4mL稀H2SO4时,溶液显中性,溶液中的溶质为硫酸钠.
(3)写出该中和反应的化学方程式:2NaOH+H2SO4═Na2SO4+2H2O.
| 滴加稀H2S04的体积/mI, | O | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| pH | 13.0 | 12.8 | 12.5 | 12.2 | 7.0 | 2.0 | 1.7 | 1.6 |
| 溶液颜色 | 蓝色 | 紫色 | 红色 | |||||

(2)当加入4mL稀H2SO4时,溶液显中性,溶液中的溶质为硫酸钠.
(3)写出该中和反应的化学方程式:2NaOH+H2SO4═Na2SO4+2H2O.
20.某同学认真分析“自然界中的氧循环”图后,产生了下列想法,其中一定错误的是( )
| A. | 动植物呼吸和燃料燃烧过程中都发生了有氧气参与的化学变化 | |
| B. | 森林里空气的氧含量高于沙漠中的空气 | |
| C. | 教室中的某个氧原子有可能来自上世纪的欧洲田园 | |
| D. | 绿色植物的作用是使自然界中的氧原子总数增加 |