��Ŀ����
8����ѧ������ϢϢ��أ���1��2016��12�£��ҹ��ں˾۱�����ȡ�����ش�ͻ�ƣ������Ǻ˾۱����Ҫԭ�ϣ��ԭ�Ӻ�����1�����Ӻ�1�����ӣ����ԭ�ӵĺ��������Ϊ1��
��2����Ȼ�����ձ������ռ�ͥ����������Ȼ������Ҫ�ɷ֣��仯ѧʽΪCH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O���Ӱ�ȫ�ĽǶȿ��ǣ�ʹ����Ȼ�����û����밲װ���������ұ�����Ӧ��װ��ǽ�ڵ��Ϸ�����Ϸ������·�������
��3��úȼ�ղ����������к��н϶�Ķ��������������̳�������Ⱦ���������ú�ˮ�ɳ�ȥ�����еĶ��������Լ��ٶԻ�������Ⱦ���乤��������ͼ��ʾ��

�������̲�����з����Ļ��Ϸ�Ӧ���£�2H2SO3+O2=2H2SO4������Դ�����á������ȷ����ۺϿ��ǣ�������е�X���ѡ����ʯ�ң�
���� ��1������ԭ���У��˵����=����������=��������������������з������
��2�����ݼ���ȼ�������˶�����̼��ˮ��д����Ӧ�ķ���ʽ��������Ȼ�����ܶȱȿ���С�������
��3��������������������Ӧ��������д����Ӧ�ķ���ʽ��
��� �⣺��1����Ϊԭ���У��˵����=����������=�������������������֪�ԭ�ӵ�ԭ�Ӻ�����1�����ӣ��ʸ�ԭ�ӵ�ԭ�Ӻ��������Ϊ1��
��2������ȼ�������˶�����̼��ˮ����Ӧ�ķ���ʽ�ǣ�CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O����Ȼ���������ϵ�ȼ������ը��������ܶȱȿ���С������ȼ��й©������Ӧ�ð�װ�ڱȽϸߵĵط����ʱ�����Ӧ�ð�װ�ڳ�����ߵ����森
�ʴ�Ϊ��CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2+2H2O���Ϸ���
��3����������������Ӧ�������ᣬ��Ӧ�ķ���ʽ��2H2SO3+O2=2H2SO4���к����������ʯ�ң�������е�X���ѡ����ʯ�ң�
�ʴ�Ϊ��2H2SO4����ʯ�ң�
���� �����ѶȲ������ջ�ѧ����ʽ����д�����ķ����Լ����������ʵ���������ȷ�����Ĺؼ���

��ϰ��ϵ�д�
 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д�
�����Ŀ
19����һ�ֻ�ѧ���ʵĻ�ѧʽNa2O2����OԪ�صĻ��ϼ�Ϊ��������
| A�� | 0 | B�� | -2 | C�� | -1 | D�� | +2 |
3��ijʵ��С�����÷�����Һ�Ʊ�K2SO4���о�CaSO4•2H2O���ȷֽ�IJ��
���Ķ����ϡ���CaSO4����ˮ��
��һ��K2SO4���Ʊ�����ͼ1��

��1����CaCO3�гɷ�ĩ��Ŀ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�
��2�����������п�ѭ��ʹ�õ�������CO2��CaCO3����д��ѧʽ����
��3������ˮ���ñ���K2SO4��Һϴ�ӷ�Ӧ�����þ����Ŀ���Ƿ�ֹK2SO4�����ܽ⣻Ϊ����˾����Ƿ�ϴ�Ӹɾ�����ȡ���һ��ϴ��Һ���ȼ���c��ѡ����ţ���ͬ���������ã������ϲ���Һ�еμ�a���۲������жϣ�
a��AgNO3��Һ b��������BaCl2��Һ c��������Ba��NO3��2��Һ
��4����Ӧ II�Ļ�ѧ����ʽΪCaSO4+H2O+2NH3+CO2=��NH4��2SO4+CaCO3����
��5����Ӧ����������ʵ��ܽ�����±�������Ϊ��Ӧ���ڳ�������ʵ�ֵ�ԭ���dz�����K2SO4���ܽ��С��
�������о�CaSO4•2H2O���ȷֽ�IJ��
��6��Ϊ�˲ⶨCaSO4•2H2O��CaCO3��������x��y��ʵ��С��������ͼ2��ʾ��װ�ã��г�����ʡ�ԣ�����ʵ�飮

��ʵ��ǰ����Ҫ���װ�õ������ԣ���װ����Ʒ��װ��A�������dz�ȥ�����е�CO2��H2O��
����֪CaSO4•2H2O��160������CaSO4��1350��ʱCaSO4��ʼ�ֽ⣻CaCO3��900��ʱ�ֽ���ȫ���ֿ���Bװ���¶�900�����ʵ�鲢�ɼ����������ݣ�
a����Ӧǰ����������Ʒ������m1g b����Ӧ�������й��������Ϊm2g
c��װ��Cʵ�������m3g d��װ��Dʵ�������m4g
ijͬѧѡ��b��d��c��d����������x��y��ֵ������װ��E����ʵ��ⶨ�����ƫС���ƫ����ƫС������Ӱ�족����
��7��CaSO4•2H2O���Ȼ���ʧȥ�ᾧˮ��CaSO4•2H2O����Է�������Ϊ172��ȡ����CaSO4•2H2O����3.44g�����ڣ�6����ʵ��װ��B�н��м��ȣ��ⶨ�����������¶ȵı仯�����ͼ3��ʾ����G�����Ļ�ѧʽ
��CaSO4•H2O��
���Ķ����ϡ���CaSO4����ˮ��
��һ��K2SO4���Ʊ�����ͼ1��

��1����CaCO3�гɷ�ĩ��Ŀ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�
��2�����������п�ѭ��ʹ�õ�������CO2��CaCO3����д��ѧʽ����
��3������ˮ���ñ���K2SO4��Һϴ�ӷ�Ӧ�����þ����Ŀ���Ƿ�ֹK2SO4�����ܽ⣻Ϊ����˾����Ƿ�ϴ�Ӹɾ�����ȡ���һ��ϴ��Һ���ȼ���c��ѡ����ţ���ͬ���������ã������ϲ���Һ�еμ�a���۲������жϣ�
a��AgNO3��Һ b��������BaCl2��Һ c��������Ba��NO3��2��Һ
��4����Ӧ II�Ļ�ѧ����ʽΪCaSO4+H2O+2NH3+CO2=��NH4��2SO4+CaCO3����
��5����Ӧ����������ʵ��ܽ�����±�������Ϊ��Ӧ���ڳ�������ʵ�ֵ�ԭ���dz�����K2SO4���ܽ��С��
| ���� | KCl | K2SO4 | NH4Cl | M |
| �ܽ��/g��25�棩 | 34.0 | 11.1 | 37.2 | 19.5 |
��6��Ϊ�˲ⶨCaSO4•2H2O��CaCO3��������x��y��ʵ��С��������ͼ2��ʾ��װ�ã��г�����ʡ�ԣ�����ʵ�飮

��ʵ��ǰ����Ҫ���װ�õ������ԣ���װ����Ʒ��װ��A�������dz�ȥ�����е�CO2��H2O��
����֪CaSO4•2H2O��160������CaSO4��1350��ʱCaSO4��ʼ�ֽ⣻CaCO3��900��ʱ�ֽ���ȫ���ֿ���Bװ���¶�900�����ʵ�鲢�ɼ����������ݣ�
a����Ӧǰ����������Ʒ������m1g b����Ӧ�������й��������Ϊm2g
c��װ��Cʵ�������m3g d��װ��Dʵ�������m4g
ijͬѧѡ��b��d��c��d����������x��y��ֵ������װ��E����ʵ��ⶨ�����ƫС���ƫ����ƫС������Ӱ�족����
��7��CaSO4•2H2O���Ȼ���ʧȥ�ᾧˮ��CaSO4•2H2O����Է�������Ϊ172��ȡ����CaSO4•2H2O����3.44g�����ڣ�6����ʵ��װ��B�н��м��ȣ��ⶨ�����������¶ȵı仯�����ͼ3��ʾ����G�����Ļ�ѧʽ
��CaSO4•H2O��
13���������ʵ����ơ���������ѧʽ�����ʵ������ȫ��ȷ���ǣ�������
| A�� | ̼���ơ����Na2CO3���� | B�� | �������ơ���ʯ�ҡ�Ca��OH��2���� | ||
| C�� | �Ȼ��ơ�ʳ�Ρ�NaCl���� | D�� | ̼�����ơ�NaHCO3���մ��� |
17�����й����з�����ѧ�仯���ǣ�������
| A�� | š���·� | B�� | д�۱��� | C�� | ʳ�︯�� | D�� | �����ֽ |
10��ʵ������������ԭ����ͭAg�����ֹ�����ʱ��ֹͣ���ȣ���ȴ���������������ΪBg������ȥ����ΪWg����ʱ����ˮ������ӦΪ��������
| A�� | $\frac{8}{9}$��A-B��g | B�� | $\frac{9}{8}$��A-B��g | C�� | 9Wg | D�� | $\frac{9}{40}$Wg |
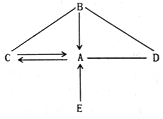 A��EΪ���л�ѧ��ͬ�������ʣ�����֮������ͼ��ʾ��ת���ͷ�Ӧ��ϵ����������ʾijһ�����ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���-����ʾ���������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ��
A��EΪ���л�ѧ��ͬ�������ʣ�����֮������ͼ��ʾ��ת���ͷ�Ӧ��ϵ����������ʾijһ�����ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���-����ʾ���������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ��