题目内容
14.写出下列反应的方程式(1)实验室用双氧水制取氧气2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(2)高锰酸钾制氧气2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(3)氯酸钾制氧气2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
(4)细铁丝在氧气中燃烧3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
(5)在加热的条件下铜丝和氧气反应2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO
(6)电解水2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(7)汽车尾气(含有CO,SO2与NO等物质)是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个“催化转换器”,其特点是使CO和NO反应,生成一种空气中含量最多的气体,另一种气体是二氧化碳.写出CO与NO反应的化学方程式是2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2
(8)发射卫星的火箭用液态联氨(N2H4)作燃料与氧气反应,燃烧后生成氮气与水.该反应的化学方程式为N2H4+O2$\frac{\underline{\;点燃\;}}{\;}$N2+2H2O质量守恒定律的定量研究对化学科学发展具有重大作用.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可
解答 解:(1)双氧水在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(4)铁丝在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(5)在加热的条件下铜丝和氧气反应,反应的化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
(6)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(7)CO和NO反应,生成一种空气中含量最多的气体,另一种气体是二氧化碳,即生成CO2和N2,其化学方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;
(8)N2H4(联氨)作燃料,在空气中燃烧后生成氮气和水,该反应的化学方程式为N2H4+O2$\frac{\underline{\;点燃\;}}{\;}$N2+2H2O.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(3)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;(4)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;(5)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;(6)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;(7)2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;(8)N2H4+O2$\frac{\underline{\;点燃\;}}{\;}$N2+2H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

| A. | 碘酒 | B. | 碳酸钙 | C. | 钢 | D. | 稀盐酸 |
| A. | 将使用后的铁锅洗涤、擦干 | |
| B. | 在铁制品表面镀一层其他金属 | |
| C. | 用碱液将铁制品表面油膜洗净后放置 | |
| D. | 在车、船表面刷油漆 |
| 液体 | 雨水 | 糖水 | 厨房清洁剂 | 厕所清洁剂 |
| pH | 5.6 | 7 | 11.8 | 2 |
(2)正常雨水的pH约为5.6的原因是水中溶解了二氧化碳生成碳酸(或二氧化碳与水反应生成碳酸);
(3)用pH试纸测定厕所清洁剂的pH时,先将pH试纸用水润湿,结果会偏大(填“偏大”、“偏小”或“无影响”).
(1)将四种溶液各取3滴分别滴入点滴板中,再向其中各滴入1滴紫色的石蕊试液,A变蓝,B不变,C、D变红.则A是NaOH(填化学式,下同),B是NaCl.
(2)为了将C、D区分出来,请你帮助小林完成剩下的实验
| 实验步骤 | 现象 | 结论 |
| 用两只试管 | 若 C中有刺激性气味产生 若 D中无现象 | C是氯化铵溶液 D是盐酸 |
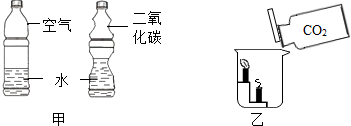
 电解水实验:a管中产生30mL的气体时,b管中同时产生气体15mL,如何检验b管中产生的气体将带火星的木条放入试管中,观察是否复燃;电解水的实验说明水是由氢元素和氧元素组成,反应的符号表达式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该反应属于分解反应.
电解水实验:a管中产生30mL的气体时,b管中同时产生气体15mL,如何检验b管中产生的气体将带火星的木条放入试管中,观察是否复燃;电解水的实验说明水是由氢元素和氧元素组成,反应的符号表达式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该反应属于分解反应.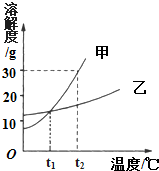 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.