题目内容
11.如图是元素周期表的一部分,请根据表中提供的信息按要求填空:| 3Li 锂 | 4Be 铍 | 5B 硼 | ①C | 7N 氮 | ②氧 | 9F 氟 | 10Ne 氖 |
| ③Na | 12Mg 镁 | ④铝 | 14Si 硅 | ⑤磷 | 16S 硫 | 17Cl 氯 | 18Ar 氩 |
(2)由①②两种元素组成的物质为CO或CO2.
(3)在元素周期表中,同一行元素最外层电子数的变化规律是由1至8逐渐增大.
分析 (1)由表中提供的信息可知,原子序数:16>⑤>14,故⑤为15号元素磷,故可推测其燃烧的化学方程式;
(2)由表中提供的信息可知,①②分别为碳元素、氧元素,故可知其组成的常用物质名称;
(3)总结归纳在元素周期表中,同一行元素最外层电子数的变化规律.
解答 解:(1)由表中提供的信息可知,原子序数:16>⑤>14,故⑤为15号元素磷,故可推测其燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)由表中提供的信息可知,①②分别为碳元素、氧元素,故可知其组成的常用物质名称为一氧化碳或二氧化碳,其化学式为:CO或CO2;
(3)总结归纳在元素周期表中,同一行元素最外层电子数的变化规律由1至8逐渐增大.
故答为:(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)CO或CO2;
(3)由1至8逐渐增大.
点评 了解元素周期表的特点及其应用;掌握化学方程式的书写方法;了解元素符号、化学式的书写及其意义.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.已知几种离子或原子的结构、带电情况及化合价如表所示:
通过此表可总结出:“带负电荷的原子属于阴离子”.还能总结出:
(1)带正电荷的原子属于阳离子;
(2)不带电荷的微粒属于原子;
(3)阴离子的化合价为负价.
| 微粒结构 示意图 | 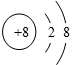 | 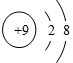 | 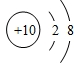 | 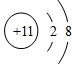 | 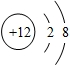 |
| 微粒类型 | 阴离子 | 阴离子 | 原子 | 阳离子 | 阳离子 |
| 微粒所带 电荷 | 2个单位负电荷 | 1个单位负电荷 | 不显电性 | 1个单位正电荷 | 2个单位正电荷 |
| 化合价 | -2 | -1 | 0 | +1 | +2 |
(1)带正电荷的原子属于阳离子;
(2)不带电荷的微粒属于原子;
(3)阴离子的化合价为负价.
6.下列情况对空气质量不会产生影响的是( )
| A. | 用氢气作燃 | B. | 焚烧垃圾 | ||
| C. | 汽车排放的尾气 | D. | 用煤和石油作燃料 |
5.潜水艇中通常用过氧化钠作供氧剂,其反应原理为2Na2O2+2CO2═O2+2X.下列有关说法正确的是( )
| A. | 该反应为置换反应 | |
| B. | Na2O2中氧元素的化合价为-2价 | |
| C. | X的相对分子质量为116 | |
| D. | 利用该反应可以维持艇内空气成分的相对稳定 |
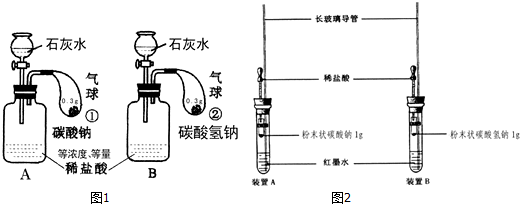
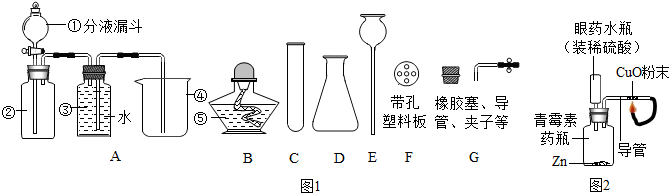
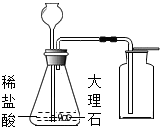 如图是实验室制取二氧化碳的一种装置.请回答下列问题:
如图是实验室制取二氧化碳的一种装置.请回答下列问题: