题目内容
4. 景德镇602所被党和国家领导人誉为“中国直升机摇篮”、“中国直升机研究发展中心”,钛合金是制作直升机重要材料,请回答下列问题:
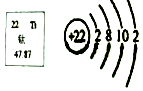
景德镇602所被党和国家领导人誉为“中国直升机摇篮”、“中国直升机研究发展中心”,钛合金是制作直升机重要材料,请回答下列问题:(1)如图是钛在元素周期表中的信息及原子结构示意图.钛的相对原子质量为47.87,它位于元素周期表第四周期.
(2)某化工企业以钛酸亚铁(FeTiO3)、焦炭、氯气为原料生成钛,钛酸亚铁中钛元素的化合价为+4.
(3)生产流程中第一步化学原理为2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO2,则X为FeCl3(填化学式);第二步:在氩气的气流中,高温下用Mg和TiCl4反应制得Ti,此过程中氩气的作用是作保护气.
分析 (1)根据元素周期表中的信息及原子结构示意图的信息来分析;
(2)根据在化合物中正负化合价代数和为零,结合钛酸亚铁的化学式进行解答即可;
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式;根据氩气的性质来分析.
解答 解:(1)由元素周期表的信息可知,钛的相对原子质量为47.87;钛原子核外有4个电子层,所以在元素周期表中位于第四周期;故填:47.87;四;
(2)铁元素显+2价,氧元素显-2价,设钛元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×3=0,则x=+4价;故填:+4;
(3)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,反应前铁、钛、氧、碳、氯原子个数分别为2、2、6、6、14,反应后的生成物中铁、钛、氧、碳、氯原子个数分别为0、2、6、6、8,根据反应前后原子种类、数目不变,则,2X分子中含有2个铁原子和6个铁原子,则每个X分子由1个铁原子和3个氯原子构成,则物质X的化学式为FeCl3.氩气的化学性质稳定,可以做保护气;故填:FeCl3;作保护气.
点评 本题难度不大,掌握化合价的原则、质量守恒定律、元素周期表与原子结构示意图的信息是正确解答本题的关键.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
15.Ga(镓)是一种活动性比铝强的金属元素,它的氧化物为Ga2O3,它对应的碱Ga(OH)3难溶于水,而GaCl3、Ga(NO3)3都易溶于水,下列各组物质能直接反应制得GaCl3的是( )
| A. | 硝酸镓溶液与氯化钙溶液 | B. | 三氧化二镓与稀盐酸 | ||
| C. | 金属镓与稀盐酸 | D. | 氢氧化镓与氯化铜溶液 |
12.下列化肥中,属于氮肥的是( )
| A. | 尿素 | B. | 硫酸钾 | C. | 磷酸二氢钙 | D. | 磷矿粉 |
9.利用如图所示装置进行相关实验能实现目标的是(部分实验步骤略)( )


| A. | 若Ⅰ中装氢氧化钠溶液,Ⅱ中装浓硫酸,则能除去碳酸氢铵受热分解产物中的二氧化碳和水蒸气,得到纯净干燥的氨气 | |
| B. | 若Ⅰ中装足量澄清石灰水,Ⅱ中装浓硫酸,则能检验气体中的CO2并测定气体中水蒸气含量 | |
| C. | 若Ⅰ中装氢氧化钠溶液,Ⅱ中装浓硫酸,则能除去CO2中混有的HCl和水蒸气 | |
| D. | 若Ⅰ中装高锰酸钾溶液,Ⅱ中装氢氧化钠溶液,则能检验并吸收SO2 |
13. 我国“神舟十号”载人飞船在轨飞行十五天,并成功与“天宫一号”对接,标志着我国已成为航天大国.如图是航天飞行器座舱内空气更新过程示意图,下列关于飞行器座舱内空气更新过程的说法错误的是( )
我国“神舟十号”载人飞船在轨飞行十五天,并成功与“天宫一号”对接,标志着我国已成为航天大国.如图是航天飞行器座舱内空气更新过程示意图,下列关于飞行器座舱内空气更新过程的说法错误的是( )
 我国“神舟十号”载人飞船在轨飞行十五天,并成功与“天宫一号”对接,标志着我国已成为航天大国.如图是航天飞行器座舱内空气更新过程示意图,下列关于飞行器座舱内空气更新过程的说法错误的是( )
我国“神舟十号”载人飞船在轨飞行十五天,并成功与“天宫一号”对接,标志着我国已成为航天大国.如图是航天飞行器座舱内空气更新过程示意图,下列关于飞行器座舱内空气更新过程的说法错误的是( )| A. | 装置Ⅰ的作用是将空气和CO2、H2O分离 | |
| B. | 装置Ⅱ中氢气和二氧化碳发生了置换反应 | |
| C. | 装置Ⅲ中水发生分解反应产生了氢气和氧气 | |
| D. | 整个过程中可以循环利用的物质是CO2和H2O |
14.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 物 质 | 所含杂质 | 除去杂质的方法 | |
| A | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| B | CO气体 | CO2 | 通过足量氢氧化钠溶液,并干燥 |
| C | Fe粉 | Cu粉 | 加入足量稀硫酸,充分反应,过滤并干燥 |
| D | CaO固体 | CaCO3 | 加水溶解,过滤 |
| A. | A | B. | B | C. | C | D. | D |
 在一次用餐中,某同学对燃料“固体酒精”产生了好奇,于是对其成分进行了探究.
在一次用餐中,某同学对燃料“固体酒精”产生了好奇,于是对其成分进行了探究.