题目内容
为了分析生铁中铁的含量,某学习小组进行了实验研究,即取6 g生铁与10%的盐酸反应,并绘制了加入盐酸的质量与放出气体质量的关系图(见下图)。
说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应。
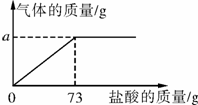
(1)铁完全反应用去盐酸的质量为________g。
(2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
(3)某同学列出了如下计算式:
生铁与盐酸反应完全时所得溶液的质量=(73+6-a) g。
小明对该计算式提出了质疑,请指出其中的错误:
________________________________________________________________________
(1)73
(2)解:设与盐酸反应的铁的质量为x。
Fe+2HCl===FeCl2+H2↑
56 73
x 73×10% g
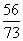 =
=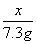
解得:x=5.6 g
生铁中铁的质量分数为=(5.6 g÷6 g)×100%=93.3%
答:略。
(3)溶液质量不包括氢气质量和剩余杂质的质量,所以还要减去杂质的质量

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
为了测定生铁中含铁量,甲、乙、丙三位同学分别取该生铁与溶质质量分数相同的稀盐酸进行实验,其中只有一位同学所取盐酸与生铁样品恰好完全反应.他们的实验数据如下表(不考虑盐酸的挥发):
| 甲 | 乙 | 丙 | |
| 所取生铁质量/g | 11.5 | 11.5 | 12 |
| 加入盐酸质量/g | 100 | 50 | 50 |
| 反应后所得气体质量/g | 0.4 | 0.4 | 0.4 |
(1)铁与盐酸恰好完全反应的是______同学的实验.
(2)计算该生铁样品中铁的质量分数.
(3)计算所用盐酸的溶质质量分数.(计算结果保留一位小数)

