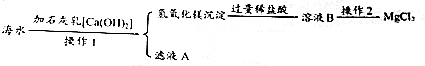题目内容
5.实验室用过氧化氢溶液100克与3克的二氧化锰制氧气,完全反应后剩余固液混合物99.3克,求原过氧化氢溶液中氢元素的质量分数( )| A. | 4.8% | B. | 10.7% | C. | 85.6% | D. | 10.2% |
分析 过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,二氧化锰作催化剂反应前后质量不变,由质量守恒定律,最终所得到的水中氢元素的质量即为原过氧化氢溶液中氢元素的质量,据此进行分析判断.
解答 解:过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,二氧化锰作催化剂反应前后质量不变,由质量守恒定律,最终所得到的水中氢元素的质量即为原过氧化氢溶液中氢元素的质量,水中氢元素的质量为(99.3g-3g)×$\frac{1×2}{1×2+16}×$100%=10.7g.
原过氧化氢溶液中氢元素的质量分数为$\frac{10.7g}{100g}×$100%=10.7%.
故选:B.
点评 本题难度不大,掌握质量守恒定律(反应前后氢元素的质量不变)并能灵活运用是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列物质中含有的原子数最多的是( )
| A. | 0.2mol氨气 | B. | 32g二氧化硫 | ||
| C. | 6.02×1022个硫酸分子 | D. | 64g铜 |
10.t℃时,向一支盛有0.074g熟石灰的试管内加入10ml水,充分振荡后,静置,试管底部仍有未溶解的白色固体,往试管中滴加1%的碳酸钠溶液,边滴加边振荡,直至沉淀质量不再变化,上层清液的质量是( )
| A. | 10.08g | B. | 10.18g | C. | 20.574g | D. | 20.674g |
6.今年4月15日是我国第一个“国家安全教育日”,下列做法不会产生安全危害的是( )
| A. | 缺碘人群食用加碘食盐 | B. | 使用工业酒精勾兑饮用酒 | ||
| C. | 将霉变米淘洗后食用 | D. | 大量使用剧毒农药,杀灭害虫 |
3.如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
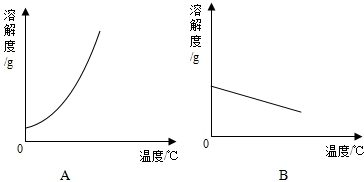
(1)依据如表数据,绘制Ca(OH)2和NaOH的溶解度曲线,如图所示能表示NaOH溶解度曲线的是A(填A或B).
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.
其中措施正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为9.1g.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数 乙<甲(填“>”、“<”或“=”).
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶,过滤.
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(填“偏大”、“偏小”或“不受影响”).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |

(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.
其中措施正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为9.1g.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数 乙<甲(填“>”、“<”或“=”).
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶,过滤.
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(填“偏大”、“偏小”或“不受影响”).
 食醋、白酒、纯碱、白糖等均为厨房用品.从中选择适当物质,进行实践活动.
食醋、白酒、纯碱、白糖等均为厨房用品.从中选择适当物质,进行实践活动.