题目内容
19. 某兴趣小组同学按如图组装仪器进行实验,请回答下列有关问题:
某兴趣小组同学按如图组装仪器进行实验,请回答下列有关问题:(1)你认为设计实验是为了测定空气中氧气的含量;
(2)实验过程中的下列操作,不妥的是④;
①检查装置气密性 ②实验前夹紧水夹 ③冷却后再打开止水夹 ④选用教室内的空气
(3)通电使红磷燃烧,燃烧的现象是红磷燃烧放出大量热产生大量白烟,该反应的文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷
(4)红磷燃烧一段时间后,自动熄灭了,原因可能是氧气耗尽
(5)冷却后,松开止水夹,观察到的现象为水进入集气瓶,进入水的体积占集气瓶容积的五分之一;
(6)用通电的方法引燃红磷与用酒精灯引燃红磷相比,优点误差小(答一点即可)
分析 (1)根据测定空气中氧气含量的实验原理进行分析判断;
(2)教室内的空气中氧气的含量偏低;
(3)根据磷燃烧的现象和反应原理分析解答;
(4)根据燃烧的条件分析解答;
(5)根据测定空气中氧气含量的实验现象分析解答;
(6)根据实验始终在密闭容器中进行五氧化二磷不会扩散到空气中进行解答;
解答 解:(1)由装置图可知该实验是为了测定空气中氧气的含量;故填:空气中氧气的含量;
(2)教室内的空气中氧气含量比正常空气中低,所以不能用教室内的空气进行实验测定,故填:④;
(3)红磷燃烧产生大量热,产生大量白烟,生成五氧化二磷,故填:红磷燃烧放出大量热产生大量白烟;磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(4)红磷燃烧一段时间后,耗尽了装置中的氧气就会熄灭,故填:氧气耗尽;
(5)实验结束后,由于集气瓶中氧气耗尽,瓶内气体压强减小,水会沿导管进入集气瓶,进入的水的体积约占集气瓶容积的五分之一;故填:水进入集气瓶进入水的体积占集气瓶容积的五分之一;
(6)用通电的方法引燃红磷使反应始终处在密闭的容器中,这样做既减小了误差,同时又减小了五氧化二磷的污染;故填:误差小(或更环保).
点评 此题综合考查空气中氧气含量的测定实验,掌握相应的实验原理和实验的注意事项以及误差分析是解关此类问题的关键.

练习册系列答案
相关题目
9.下列物质都属于纯净物的是( )
| A. | 24K金、洗衣粉、雪碧汽水 | B. | 吸入的空气、粗盐、金刚石 | ||
| C. | 冰水、苏打、干冰 | D. | 石灰石、钢、加铁酱油 |
10.下列对碳和碳的氧化物的说法不正确的是( )
| A. | 活性炭、木炭都具吸附性 | |
| B. | 一氧化碳和二氧化碳都有毒 | |
| C. | 木炭、一氧化碳在一定条件下都能与氧化铜反应 | |
| D. | 金刚石、石墨和C60都是碳元素的单质 |
4.欲除去下列物质中的少量杂质,所用试剂正确的是( )
| 选项 | 物质 | 杂质 | 试剂 |
| A | CO2 | SO2 | NaOH溶液 |
| B | KCl | K2SO4 | Ba(OH)2溶液 |
| C | CO2 | CO | Ca(OH)2溶液 |
| D | CaCO3 | CuSO4 | H2O |
| A. | A | B. | B | C. | C | D. | D |
8.金属用途广泛,其结构和性质等是化学的重要研究内容.
(1)如图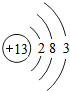 是铝的原子结构示意图.下列说法不正确的是C.
是铝的原子结构示意图.下列说法不正确的是C.
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了图1实验,并对溶液A和固体B的成分进行了分析和实验探究.
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2②有Zn (NO3)2、AgNO3③有 Zn (NO3)2、Cu(NO3)2
④有Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是(填标号),其理由是:②,Zn应先与AgNO3反应,后与Cu(NO3)2反应,当有AgNO3剩余时,溶质中一定含有Cu(NO3)2.
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整.
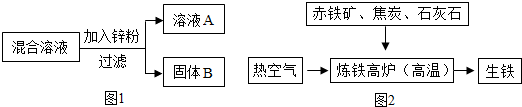
(3)图2是工业炼铁示意图.其中,焦炭的作用是燃烧提供能量并制取制取CO;试写出有铁生成的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(4)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁.现有废硫酸49t(其H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?
(1)如图
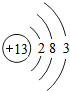 是铝的原子结构示意图.下列说法不正确的是C.
是铝的原子结构示意图.下列说法不正确的是C.A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了图1实验,并对溶液A和固体B的成分进行了分析和实验探究.

【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2②有Zn (NO3)2、AgNO3③有 Zn (NO3)2、Cu(NO3)2
④有Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是(填标号),其理由是:②,Zn应先与AgNO3反应,后与Cu(NO3)2反应,当有AgNO3剩余时,溶质中一定含有Cu(NO3)2.
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整.
| 实验步骤 | 现象 | 有关反应的化学方程式 |
| 取少量固体B, 滴加稀盐酸 | 有气泡 产生 | Zn+2HCl=ZnCl2+H2↑ |
(4)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁.现有废硫酸49t(其H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?

