题目内容
10.现有下列物质①硫酸钠、②烧碱、③纯碱、④干冰、⑤石墨、⑥盐酸,根据要求写出相应物质的化学式:单质C,氧化物CO2,酸HCl,碱NaOH,盐Na2SO4、Na2CO3.
分析 首先根据题意确定物质的化学名称,然后根据题目所提供的物质、书写化学式的方法和步骤写出物质的化学式即可.
解答 解:单质是由一种元素组成的纯净物,提供的物质中,石墨属于单质,故填:C;
氧化物是由两种元素组成的化合物,并且其中一种为氧元素,提供的物质中,干冰属于氧化物;故填:CO2;
酸是指在电离时产生的阳离子全部是氢离子的化合物,根据提供的盐酸符合要求,其化学式为:HCl;故填:HCl;
碱是指在电离时产生的阴离子全部是氢氧根离子的化合物,根据提供的烧碱(氢氧化钠)属于碱,其化学式为:NaOH.故填:NaOH;
盐是由金属离子和酸根离子组成的化合物,根据提供的元素硫酸钠、纯碱(碳酸钠)属于盐,故填:Na2SO4、Na2CO3.
点评 本题难度不大,熟练掌握单质、氧化物、酸、碱、盐的特征,常见物质的组成及化学式的书写是正确解答此类题的关键所在.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.“人造空气”帮助人类实现了“太空漫步”的梦想,其中含有70%的N2、20%以上的O2、还有CO2等.下列说法正确的是( )
| A. | “人造空气”中的氮气含量比空气中的氮气含量高 | |
| B. | 燃着的蜡烛在“人造空气”中会熄灭 | |
| C. | 可以利用反应2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,测定“人造空气”中O2的含量 | |
| D. | “人造空气”若只含有O2会更有益于人的呼吸 |
1.检验集气瓶中的氧气是否收集满,应将带火星的木条( )
| A. | 伸入集气瓶底部 | B. | 伸入集气瓶中部 | C. | 伸入集气瓶口内 | D. | 伸到集气瓶口 |
18.下列化肥不溶于水的是( )
| A. | 磷矿粉 | B. | 氯化铵 | C. | 碳酸氢铵 | D. | 硫酸钠 |
5.下列与生活相关的说法中错误的是( )
| A. | 工业用盐亚硝酸钠可以代替食盐用于烹任 | |
| B. | 碳酸钙可以用作补钙剂 | |
| C. | 碳酸氢钠是焙制糕点所用发酵粉的主要成分之一 | |
| D. | 氯化钠所提供的氯离子是胃液的主要成分,具促生盐酸、帮助消化和增进食欲的作用 |
2.下列四个图形图象中能正确反应其对应实验操作的是( )
| A. | 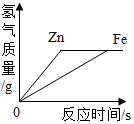 向足量的锌粉和铁粉中分别加入相同质量相同质量分数的稀盐酸 | |
| B. | 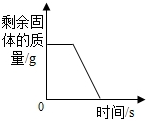 煅烧一定质量的石灰石 | |
| C. | 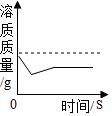 向饱和的石灰水中加入一定质量氧化钙 | |
| D. | 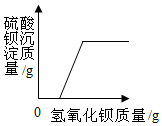 向一定质量的稀硫酸和硫酸铜混合溶液中滴加氢氧化钡溶液 |
19.下表是元素周期表的一部分,则下列叙述正确的是( )
| 11Na 钠 | 12Mg 镁 | 13Al 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | 17Cl 氯 | 18Ar 氩 | |
| 19K 钾 | 20Ca 钙 | … |
| A. | 硫原子的核外电子排布是 | |
| B. | 12号元素的离子符号是Mg+2 | |
| C. | 钙元素的相对原子质量为20 | |
| D. | 表中左边是金属元素,右边是非金属元素 |
