题目内容
15.化学世界千变万化.请写出下列反应的化学符号表达式,并回答有关问题.(1)加热高锰酸钾:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,反应后锰元素的化合价降低(填“升高”、“降低”或“不变”).
(2)加热碳酸氢铵:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2+NH3↑,碳酸氢铵应保存在广口瓶中(填“细口瓶”、“广口瓶”或“滴瓶”中).
(3)镁条在空气中燃烧:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,燃烧的镁条应用坩埚钳夹持置于石棉网上.
(4)将二氧化碳通入紫色石蕊试液变红:CO2+H2O=H2CO3.该反应属于化合反应类型(填基本反应类型).
(5)将二氧化锰放入双氧水中:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.该反应属于放热反应(填“吸热”或“放热”).
分析 (1)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(2)根据碳酸氢铵在加热的条件下生成氨气、水和二氧化碳进行分析;
(3)根据镁和氧气在点燃的条件下生成氧化镁进行分析;
(4)根据二氧化碳和水反应生成碳酸进行分析;
(5)根据过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析.
解答 解:(1)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,反应后锰元素的化合价降低;
(2)碳酸氢铵在加热的条件下生成氨气、水和二氧化碳,化学方程式为:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2+NH3↑,碳酸氢铵应保存在广口瓶中;
(3)镁和氧气在点燃的条件下生成氧化镁,化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,燃烧的镁条应用坩埚钳夹持置于石棉网上;
(4)二氧化碳和水反应生成碳酸,化学方程式为:CO2+H2O=H2CO3,该反应属于化合反应;
(5)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应属于放热反应.
故答案为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,降低;
(2)NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2+NH3↑,广口瓶;
(3)2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,坩埚钳;
(4)CO2+H2O=H2CO3,化合;
(5)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,放热.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案(1)收集竹子中的气体.
小黄提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体.
小州提出:可用注射器从竹子中抽取气体.
大家认为两人的想法都可行,于是分为A、B两组,在相同的条件下,A组采用小黄的取气方法,B组采用小州的取气方法,分别完成下面的实验.
(2)检验气体中是否含有二氧化碳气体.
| 实验步骤 | 实验现象 | 实验结论及解释 |
| 在所取气体中加入澄清石灰水 | 澄清石灰水变浑浊 | 含有二氧化碳 |
【查阅资料】
①红磷的着火点(即燃烧所需最低温度)为240℃,白磷的着火点为40℃;
②通常情况下,1体积水可以溶解1体积的二氧化碳.
【设计实验】
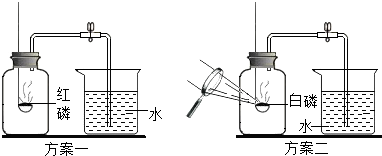
同学们设计了如图所示的方案一和方案二来测定收集到的竹子中的气体的氧气含量.
【进行实验】按上述两个方案进行多次实验.
【反思与评价】
①两个方案实验时第一步操作均是检查装置气密性
②按照方案二探究时,凸透镜照射后,广口瓶中的实验现象是白磷剧烈燃烧,产生大量白烟,发生反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,打开止水夹后,实验现象是水进入集气瓶,如果没有冷却至室温,就打开止水夹,则实验结果将偏小(填偏大、偏小或不变).
两个方案的实验测定结果不同,测定结果比较准确的是方案二,原因是方案一中,燃烧匙伸入集气瓶中时,瓶内气体受热膨胀导致部分气体逸出.
③经过A、B两组同学们的实验,A组测得的含氧量总是大于B组的,你认为原因是A组收集气体时部分二氧化碳溶于水中.
【提出问题Ⅰ】固体酒精是固态的酒精吗?
【查阅资料Ⅰ】酒精,学名乙醇,化学式为C2H6O,熔点为-114.1℃,沸点为78.5℃,易溶于水,能与水以任意比互溶.
【实验探究Ⅰ】取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残留了少量白色固体.
【提出问题Ⅱ】白色固体是什么呢?
【查阅资料Ⅱ】以硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,将酒精填充在硬脂酸钠骨架间隙中,即可得到固体酒精.固体酒精在较高温度下燃烧时,硬脂酸钠可完全转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水.
【实验探究Ⅱ】验证白色固体的成分.回答下列问题:
(1)即使不了解固体酒精的制作方法,也能判断固体酒精不是固态的酒精,因为酒精的熔点为-114.1℃,通常情况下不可能是固体.
(2)酒精完全燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(3)根据资料Ⅱ可以猜测白色固体可能是NaOH和Na2CO3的混合物,请你设计一个实验方案加以验证,将实验操作和支持结论的现象填写在下表中.
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取适量白色固体于试管中,加入足量水,再加入过量氯化钡溶液;②取试管中上层清液于另一试管中,滴加酚酞试液. | ①产生白色沉淀;②溶液变红色. | 白色固体是NaOH和Na2CO3的混合物 |
| A. | 都属于氧化物 | B. | 都含有氧气 | C. | 都含有氧分子 | D. | 都含有氧元素 |
| A. | 按质量计算,空气中约含氮气78%,氧气21%,其他气体和杂质约占1% | |
| B. | 少量有害气体进入空气中,依靠大自然的自净能力,空气仍能保持洁净 | |
| C. | 空气是一种重要的天然资源,也是常见的混合物 | |
| D. | 空气中的稀有气体之所以曾被称为“惰性气体”,是由于它们化学性质极为稳定 |



