��Ŀ����
����������������ҽ����е�����ӵȹ�ҵ��ijʵ����ȤС��ӹ����ɼ���Һ����FeSO4������ZnSO4��MgSO4���������������������Ʊ�ʵ�顣
���Ķ����ϡ�
��1��25��ʱ��ȥ�����������pH��Χ�����
Zn��OH��2 | Fe��OH��2 | Mg��OH��2 | |
��ʼ������pH | 5.7 | 7.6 | 10.4 |
������ȫ��pH | 8.0 | 9.6 | 12.4 |
��2��25��ʱ��Zn��OH��2������pH��10.5�ļ���Һ��
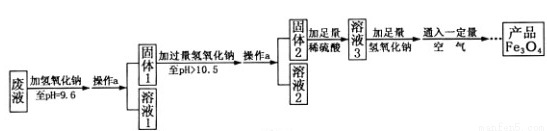
��3���Ʊ�Fe3O4��ʵ���������£�
���ش����⡿
��1������Һ�м�������������Һ���ɳ����Ļ�ѧ����ʽΪ ��дһ�����ɣ���
��2������a������Ϊ ���ò�����Ҫ�IJ����������ձ����������� �ȡ��������ڴ˲����е���Ҫ������ ��
��3����Һ1���������� ������д���֣�����Һ3�������ʵ���Ҫ�ɷ�Ϊ ��
��4����ʵ��ȡ��Һ100g�����յõ���Ʒ��������������Ϊ3.48g����ԭ��Һ�������������ʵ��������������� ����ȷ��0.01%����
��2 NaOH+ ZnSO4= Zn��OH��2�� +Na2SO4��2 NaOH+ FeSO4= Fe��OH��2�� +Na2SO4�ƹ��ˡ�©�������������裩������þ�������ơ��������ơ�������þ�����ּ��ɣ����������� ��6.84% ����������1����һ��������������PH=9.6������Ķ����Ͽ�֪���������ֳ��������Ƿֱ���Zn��OH��2��Fe��OH��2�����Ҷ���ȫ����������д2 NaOH+ ZnSO... ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д� Ʒѧ˫�ž�ϵ�д�
Ʒѧ˫�ž�ϵ�д� Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д���Ƭ�ı�ǩ��ͼ��ʾ���Ҹ�Ƭ��ֻ��̼����к��и�Ԫ�ء�Ϊ�ⶨ����ʵ�ĺ�������С��ȡ10Ƭ��Ƭ����ʢ����������ձ��У���ַ�Ӧ���ٳ�ȡ�ձ���ʣ�������������
С����������ʵ�飬�������±���
���ʵ�����/ g | ��һ�� | �ڶ��� | ������ | ƽ��ֵ |
��Ӧǰ���ձ�+���� | 22 | 22 | 22 | 22 |
10Ƭ��Ƭ | 8 | 8 | 8 | 8 |
��Ӧ���ձ�+ʣ���� | 26.7 | 26.5 | 26.9 | 26.7 |
��1������ʽ����ÿƬ�˸�Ƭ��̼��Ƶ�����_______��
��2����ͨ������˵���˱�ǩ�еĺ������Ƿ����_______��
3.3g�� �˱�ǩ�еĺ������������� �������������йػ�ѧʽ�ļ��㡢���û�ѧ����ʽ�ļ��㼴����ȷ����⣬���������غ㶨�ɼ����������̼�������������ȷ�����Ĺؼ��� ��1�����ɶ�����̼���������Ϊ��22g+8g-26.7g=3.3g�� ��10Ƭ��Ƭ��̼��Ƶ�����Ϊx�� CaCO3+2HCl=CaCl2+H2O+CO2�� 100 44 x 3.3g x=...