题目内容
甲酸(HCOOH)通常是一种无色易挥发的液体,它在浓硫酸作用下易分解,反应方程式为:HCOOH
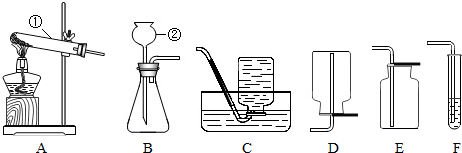
CO↑+H2O,某课外活动小组的同学欲用该反应来制取CO,并还原黑色的氧化铜粉末.现有下列仪器或装置供选择:
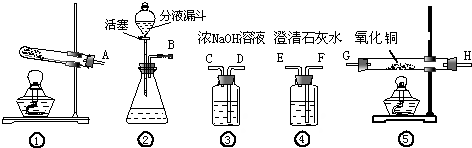
(1)用甲酸滴入浓硫酸的方法制取CO,应选 (填序号)装置;如果要除去CO中混有少量甲酸气体,最好选择图中 (填序号)进行洗气.
(2)用上述方法制取的CO还原氧化铜,并检验气体产物,则各仪器的接口连接顺序为: (填字母).
(3)从开始加热到实验结束,氧化铜粉末的颜色变化为 ,反应方程式为 .
(4)在该制取CO的反应中,浓硫酸所起的是 作用.
| ||

(1)用甲酸滴入浓硫酸的方法制取CO,应选
(2)用上述方法制取的CO还原氧化铜,并检验气体产物,则各仪器的接口连接顺序为:
(3)从开始加热到实验结束,氧化铜粉末的颜色变化为
(4)在该制取CO的反应中,浓硫酸所起的是
考点:一氧化碳的化学性质,常见气体的检验与除杂方法,气体的净化(除杂),书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途
分析:(1)根据分液漏斗的用途分析选择用甲酸滴入浓硫酸的装置;根据氢氧化钠和氢氧化钙的溶解性分析除去CO中混有少量甲酸气体应用的装置;
(2)用一氧化碳CO还原氧化铜.应先除去出甲酸气体,再还原氧化铜,最后用澄清的石灰水检验生成的二氧化碳,据此分析各仪器的接口连接顺序;
(3)根据反应物、生成物的颜色分析现象,写出反应的方程式;
(4)根据浓硫酸具有脱水性分析.
(2)用一氧化碳CO还原氧化铜.应先除去出甲酸气体,再还原氧化铜,最后用澄清的石灰水检验生成的二氧化碳,据此分析各仪器的接口连接顺序;
(3)根据反应物、生成物的颜色分析现象,写出反应的方程式;
(4)根据浓硫酸具有脱水性分析.
解答:解:(1)向甲酸中滴加浓硫酸液体,应通过分液漏斗加入.所以,应该选择②装置;氢氧化钠溶液、氢氧化钙溶液都能够吸收CO中混有的少量甲酸气体,但是氢氧化钠溶液的吸收能力比氢氧化钙溶液强.所以,应选装置③;
(2)生成的一氧化碳气体从B中排出,从D进入氢氧化钠溶液除去甲酸气体,从C中排出;再从G进入,在加热的条件下.一氧化碳还原氧化铜,气体再从H排出,最后从F进入氢氧化钙溶液中,检验有二氧化碳生成.所以,各仪器的接口连接顺序为:B D C G H F.
(3)在加热的条件下,氧化铜被还原成铜,所以,从开始加热到实验结束,氧化铜粉末的颜色变化为:黑色变红色,反应方程式为:CuO+CO
Cu+CO2.
(4)由题意可知,在该制取CO的反应中,浓硫酸使甲酸脱水生成了一氧化碳,起到脱水的作用.
故答为:(1)②,③;(2)B D C G H F;(3)黑色变红色,CuO+CO
Cu+CO2;(4)脱水.
(2)生成的一氧化碳气体从B中排出,从D进入氢氧化钠溶液除去甲酸气体,从C中排出;再从G进入,在加热的条件下.一氧化碳还原氧化铜,气体再从H排出,最后从F进入氢氧化钙溶液中,检验有二氧化碳生成.所以,各仪器的接口连接顺序为:B D C G H F.
(3)在加热的条件下,氧化铜被还原成铜,所以,从开始加热到实验结束,氧化铜粉末的颜色变化为:黑色变红色,反应方程式为:CuO+CO
| ||
(4)由题意可知,在该制取CO的反应中,浓硫酸使甲酸脱水生成了一氧化碳,起到脱水的作用.
故答为:(1)②,③;(2)B D C G H F;(3)黑色变红色,CuO+CO
| ||
点评:解答好本题首先要明确装置的作用,此外掌握一氧化碳还原氧化铜的反应相关内容,洗气装置中导管要长进短出才能正确分析解答.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
某学生在称量时,误将药品与砝码对调位置放入托盘内,他读出的数值为12.4g(1g以下用游码),那么该固体药品的实际质量是( )
| A、12.4g | B、12g |
| C、11.6g | D、7.6g |
下列药品未经密封保存,敞放置一段时间后,质量增加并发生化学反应的是( )
①苛性钠
②碳酸钠晶体
③浓盐酸
④浓硫酸
⑤熟石灰.
①苛性钠
②碳酸钠晶体
③浓盐酸
④浓硫酸
⑤熟石灰.
| A、①③ | B、②④ | C、①⑤ | D、④⑤ |