题目内容
9.如图是某化工厂设计的基础化工生产流程,回答问题.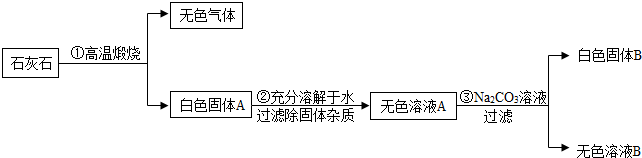
(1)白色固体A中,可用作某些气体干燥剂的成分是氧化钙;
(2)按生产流程,该化工厂最终生产出的产品有纯净碳酸钙粉末,还有氢氧化钠和二氧化碳;
(3)如果③反应Na2CO3溶液的用量不足,向无色溶液B中通入二氧化碳气体,会观察到的现象是溶液变浑浊;
(4)如果③反应NaCO3溶液使用过得,对无色溶液B的有关说法中,正确的是AD.
A.溶液中含有的阳离子全部是钠离子
B.向其中滴加稀盐酸,一定有气泡产生
C.可用来鉴别CaCl2溶液和Ba(OH)2溶液
D.向其中滴加石灰水到不再产生沉淀并过滤,滤液中只含有一种溶质.
分析 根据碳酸钙高温煅烧生成二氧化碳和氧化钙,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠进行解答.
解答 解:(1)碳酸钙高温煅烧生成二氧化碳和氧化钙,氧化钙能吸水,所以可用干燥剂;故填:氧化钙;
(2)碳酸钙高温煅烧生成二氧化碳和氧化钙,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,所以按生产流程,该化工厂最终生产出的产品有纯净碳酸钙粉末,还有氢氧化钠和二氧化碳;故填:氢氧化钠和二氧化碳;
(3)如果③反应Na2CO3溶液的用量不足,那么氢氧化钙会有剩余,所以向无色溶液B中通入二氧化碳气体,会观察到的现象是溶液变浑浊;故填:溶液变浑浊;
(4)如果③反应NaCO3溶液使用过量,那么无色溶液B中含有氢氧化钠和碳酸钠.
A.溶液中含有的阳离子全部是钠离子,故A正确;
B.向其中滴加稀盐酸,如果盐酸的量少,不一定会放出二氧化碳气体,所以不一定有气泡产生,故B错误;
C.碳酸钠和氯化钙、氢氧化钡都会生成白色沉淀,所以不能用来鉴别CaCl2溶液和Ba(OH)2溶液,故C错误;
D.氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以向其中滴加石灰水到不再产生沉淀并过滤,滤液中只含有一种溶质,就是氢氧化钠,故D正确.
故选:AD.
点评 本题难度不大,掌握碳酸钙、氧化钙、氢氧化钙的相互转化并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
4.某金属制品厂清洗金属后产生一种黄色废液,小刚和小强欲对其成分进行探究.请你参与探究,填写空格:
【查阅资料】工业上通常使用稀盐酸或稀硫酸清洗金属表面的锈迹.
【猜想与假设】小刚认为废液中只含有硫酸铁;小强认为废液中可能还含有氯化铁.
【进行实验】小刚的实验报告如下:
【反思与改进】
(1)小强通过改进小刚的实验,证明了自己的猜想是正确的.小强的实验操作要点是:取少量澄清废液,先加入足量硝酸钡溶液,过滤,向滤液中滴加硝酸银溶液,产生白色沉淀.
(2)通过分析小刚的实验现象,简要说明他们探究过程中的不足之处:未考虑废液中含有酸.
【查阅资料】工业上通常使用稀盐酸或稀硫酸清洗金属表面的锈迹.
【猜想与假设】小刚认为废液中只含有硫酸铁;小强认为废液中可能还含有氯化铁.
【进行实验】小刚的实验报告如下:
| 实验步骤 | 实验现象 | 解释与结论 |
| ①取少量澄清废液于试管中,逐滴加入足量氢氧化钾溶液 | 刚开始没有明显现象,过一段时间后产生红褐色沉淀 | 生成红褐色沉淀的是氢氧化铁 |
| ②过滤,向滤液中滴加氯化钡溶液至恰好完全反应 | 产生白色沉淀 | 废液中一定含有硫酸铁 |
(1)小强通过改进小刚的实验,证明了自己的猜想是正确的.小强的实验操作要点是:取少量澄清废液,先加入足量硝酸钡溶液,过滤,向滤液中滴加硝酸银溶液,产生白色沉淀.
(2)通过分析小刚的实验现象,简要说明他们探究过程中的不足之处:未考虑废液中含有酸.
18.下列除去杂质的方法中,错误的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | CO(CO2) | 通过足量的NaOH溶液、干燥 |
| D | FeSO4溶液(H2SO4) | 加入足量Fe粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
19.推理是化学学习中常见的思维方法,下列推理正确的是( )
| A. | 碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性 | |
| B. | 中和反应一定有盐生成,所以有盐生成的反应一定是中和反应 | |
| C. | 离子是带电荷的原子或原子团,所以带电荷的微粒一定是离子 | |
| D. | 溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小 |
