题目内容
17.下列有关物质性质与用途分析正确的是AA、一氧化碳有还原性,可用于冶炼金属
B、氧气有可燃性,可用于燃烧
C、聚乙烯塑料有热固性,受热易变形
D、氢气有可燃性性,可用作燃料.
分析 A、根据一氧化碳具有还原性进行分析;
B、根据氧气的性质进行分析;
C、根据聚乙烯属于典型的热塑性塑料进行分析;
D、根据氢气的性质进行分析.
解答 解:A、一氧化碳具有还原性,可与金属氧化物发生氧化-还原反应,可用于冶炼金属;故A正确;
B、氧气能支持燃烧,本身不具有可燃性,故B错误;
C、通常的聚乙烯,包括高低压聚乙烯属于典型的热塑性塑料,故C错误;
D、氢气有可燃性性,可用作燃料;故D正确;
故选A,D补充可燃性.
点评 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.

练习册系列答案
相关题目
8.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和NaOH溶液中,观察到如表异常实验现象:
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
【提出问题】
实验Ⅰ中蓝色沉淀为什么消失?
【查阅资料】
①氢氧化铜在室温下稳定,70℃~80℃时分解(产物有氧化铜).
②铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
针对实验Ⅰ中蓝色沉淀为什么消失,同学们提出如下两个猜想:
猜想①:蓝色沉淀消失可能是氢氧化铜发生分解反应.
猜想②:蓝色沉淀消失可能是氢氧化铜溶解在NaOH溶液中,形成亮蓝色溶液.
甲同学认为猜想①不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
【实验验证】
乙同学为验证猜想②,进行了如表实验.
【解释与结论】
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
(3)进一步查阅资料可知,氢氧化铜在NaOH溶液中溶解生成铜酸钠,反应的化学方程式为2NaOH+Cu(OH)2=Na2Cu(OH)4.
【反思与评价】
针对实验Ⅱ,丙同学推测,饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| Ⅰ | 第1~6滴 | 有蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| Ⅱ | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,但沉淀很快变成黑色 |
【提出问题】
实验Ⅰ中蓝色沉淀为什么消失?
【查阅资料】
①氢氧化铜在室温下稳定,70℃~80℃时分解(产物有氧化铜).
②铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
针对实验Ⅰ中蓝色沉淀为什么消失,同学们提出如下两个猜想:
猜想①:蓝色沉淀消失可能是氢氧化铜发生分解反应.
猜想②:蓝色沉淀消失可能是氢氧化铜溶解在NaOH溶液中,形成亮蓝色溶液.
甲同学认为猜想①不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
【实验验证】
乙同学为验证猜想②,进行了如表实验.
| 实验操作 | 实验现象 |
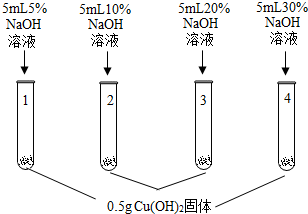 | 1号试管,… 2号试管,蓝色固体不消失 3号试管,蓝色固体减少 4号试管,蓝色固体消失,得到亮蓝色溶液 |
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
(3)进一步查阅资料可知,氢氧化铜在NaOH溶液中溶解生成铜酸钠,反应的化学方程式为2NaOH+Cu(OH)2=Na2Cu(OH)4.
【反思与评价】
针对实验Ⅱ,丙同学推测,饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
12.预防佝偻病或骨质疏松需要补充的元素是( )
| A. | 铁 | B. | 碘 | C. | 钙 | D. | 锌 |
2.元素周期表中,同周期元素的结构和性质呈现一定的规律性变化.如表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出).
请回答下列问题:
(1)⑤处是+7,⑥处是-3;
(2)③处的数值范围是1.02-1.17;
(3)由表可得到的其中一条规律是:第三周期元素(Na~Cl)的最高正价数等于最外层电子数;
(4)元素①的原子序数是13,①和②形成的化合物的化学式为Al2S3.
| 元素 | Na | Mg | ① | Si | P | ② | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(×10-10m) | 1.86 | 1.60 | 1.43 | 1.17 | ③ | 1.02 | 0.994 |
| 最高正价 | +1 | +2 | ④ | +4 | +5 | +6 | ⑤ |
| 最低负价 | -4 | ⑥ | -2 | -1 |
(1)⑤处是+7,⑥处是-3;
(2)③处的数值范围是1.02-1.17;
(3)由表可得到的其中一条规律是:第三周期元素(Na~Cl)的最高正价数等于最外层电子数;
(4)元素①的原子序数是13,①和②形成的化合物的化学式为Al2S3.
6.分类法是化学学习的重要方法.下列说法正确的是( )
| A. | 烧碱、纯碱、热石灰是常见的碱 | |
| B. | 蛋白质、合成纤维、油脂是常见的营养物质 | |
| C. | 生石灰、碱石灰、浓硫酸都可用作干燥剂 | |
| D. | 尿素、硝酸钾、磷酸二氢铵都可作复合肥料 |
7.甲和乙可以合成清洁燃料丙,微观过程如下图.下列说法不正确的是( )
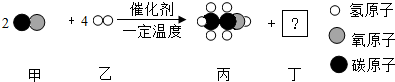

| A. | 丁的化学式为H2O2 | |
| B. | 丙中C、H、O元素质量比为12:3:8 | |
| C. | 一定浓度的丙溶液可作消毒剂 | |
| D. | 该反应体现在一定条件下无机物可转化为有机物 |
 近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此,国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.
近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此,国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.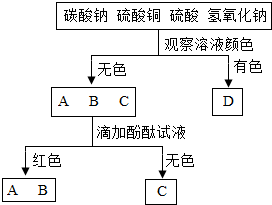 有四种常见的酸、碱或盐的溶液,用图所示的化学分析方法鉴别它们:
有四种常见的酸、碱或盐的溶液,用图所示的化学分析方法鉴别它们: