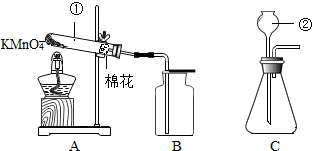
题目内容
8.能源、环境与人类生活和社会发展密切相关.(1)目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和天然气.
(2)甲、乙两个城市全年雨水的月平均pH变化如图1.下列说法正确的是CD(填字母).
A.甲城市受酸雨的影响较严重
B.pH小于6的降雨称为酸雨
C.煤的大量燃烧是造成酸雨的主要原因之一
D.大力推广使用脱硫煤可以减少酸雨的形成
(3)二氧化氮进入大气后与雨水作用,可能形成硝酸型酸雨,硝酸的化学式为HNO3.氨气进入大气后与雨水作用,
(4)可能形成“碱雨”,“碱雨”中碱的化学式为NH3•H2O.
(5)“碱雨”中的碱和盐酸发生中和反应生成一种可用作氮肥的 铵盐,其化学式为NH4Cl.
(6)图2是某反应的微观示意图,通过该反应可以将氨气转化.若D为空气中体积分数最大的气体,则生成C和D 的质量比为27:14.
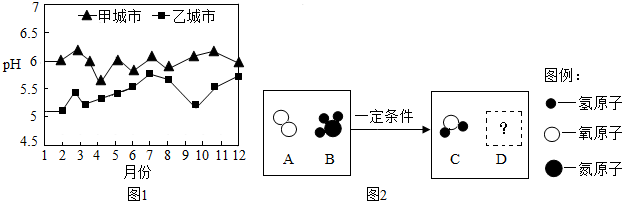
分析 (1)根据化石燃料包括煤、石油、天然气进行分析;
(2)A、根据溶液酸碱性和pH值之间的关系进行分析;
B、根据pH小于5.6的降雨称为酸雨进行分析;
C、根据煤燃烧会产生大量的二氧化硫进行分析;
D、根据大力推广使用脱硫煤可以减少二氧化硫的排放进行分析;
(3)根据化学式的正确书写方法进行分析;
(4)根据氨气进入大气后与雨水作用,可能形成氨水解答;
(5)根据氨水和盐酸反应生成氯化铵和水解答;
(6)根据D为空气中体积分数最大的气体,所以D是氮气,氨气和氧气反应生成氮气和水进行分析.
解答 解:(1)化石燃料包括煤、石油、天然气;
(2)A、溶液酸碱性和pH值之间的关系,甲城市的pH值大于乙产生,所以乙城市受酸雨的影响较严重,故A错误;
B、pH小于5.6的降雨称为酸雨,故B错误;
C、煤燃烧会产生大量的二氧化硫,故C正确;
D、大力推广使用脱硫煤可以减少二氧化硫的排放,故D正确;
故选:CD.
(3)二氧化氮进入大气后与雨水作用,可能形成硝酸型酸雨,硝酸的化学式为HNO3,
(4)氨气进入大气后与雨水作用,可能形成氨水,氨水的化学式为NH3•H2O,
(5)氨水和盐酸反应生成氯化铵和水,化学式为NH4Cl;
(6)D为空气中体积分数最大的气体,所以D是氮气,氨气和氧气反应生成氮气和水,化学方程式为:
4NH3+3O2$\frac{\underline{\;一定条件\;}}{\;}$6H2O+2N2
108 56
所以生成C和D的质量比为108:56=27:14.
故答案为:
(1)天然气;
(2)CD;
(3)HNO3,
(4)NH3•H2O,
(5)NH4Cl;
(6)27:14.
点评 化石燃料的燃烧能够产生大量的二氧化硫、氮氧化物,这些物质是形成酸雨的重要物质,因此减少化石燃料的使用,综合利用化石燃料有利于减少酸雨的产生.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | c═a+b | B. | c═2 b-a | C. | c═a+2 b | D. | c═2 a-b |
| A. | 味精 | B. | 食盐 | C. | 白醋 | D. | 芝麻油 |
①H2②O2③CO2④SO2⑤CO ⑥HCl ⑦NH3.
| A. | ①② | B. | ①②⑤⑦ | C. | 全部 | D. | ①②⑤ |
| A. | 野外遭遇火灾,逆风而行,更方便逃离火海 | |
| B. | 天然气泄漏报警器安装在炉灶下方,更有利于及时发现泄漏 | |
| C. | 炒菜时油锅起火,可立即倒入蔬菜 | |
| D. | 将木柴架空有利于篝火烧得更旺 |
 以下是小文在家里找到的一些物品.
以下是小文在家里找到的一些物品.