题目内容
10. 实验室用足量二氧化锰与浓盐酸加热制取氯气,当反应时氯化锰与氯化氢混合溶液中氯化氢的质量分数降低至20%,反应停止.反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.
实验室用足量二氧化锰与浓盐酸加热制取氯气,当反应时氯化锰与氯化氢混合溶液中氯化氢的质量分数降低至20%,反应停止.反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑.(已知:混合溶液中,某一溶质的质量分数=$\frac{该溶质的质量}{混合溶液的质量}$×100%)
(1)二氧化锰中,锰元素与氧元素的质量比为55:32.
(2)实验小组欲废物再利用,若要将一定量上述制氯气的剩余液体配成含氯化氢8%的除锈液,计算配制80g该除锈液所需上述反应剩余液体和所加水的质量.
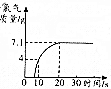
(3)制取氯气的质量与时间如图所示,测得反应停止时,剩余溶液质量为101.6g.计算制氯气实验中所用浓盐酸的溶质的质量分数.
分析 (1)根据元素质量比等于相对原子质量和原子个数乘积的比值进行分析;
(2)根据溶液稀释前后溶质质量不变进行分析;
(3)根据化学方程式和题中的数据进行计算.
解答 解:(1)二氧化锰中,锰元素与氧元素的质量比为55:(2×16)=55:32;
(2)需反应剩余液体质量为:$\frac{80g×8%}{20%}$=32g,需要水的质量为:80g-32g=48g;
(3)设参加反应的氯化氢质量为x,二氧化锰为y,
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑
87 146 71
y x 7.1g
$\frac{146}{x}$=$\frac{71}{7.1g}$=$\frac{87}{y}$
x=14.6g
y=8.7g
所以制氯气实验中所用浓盐酸的溶质的质量分数为:$\frac{14.6g+101.6g×20%}{101.6g+7.1g-8.7g}$×100%=34.92%.
故答案为:(1)55:32;
(2)需反应剩余液体质量为32g,需要水的质量为48g;
(3)所以制氯气实验中所用浓盐酸的溶质的质量分数为34.92%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
18.学习化学让我们有了很多收获,下列归纳总结完全正确的一组是( )
| A、认识物质俗名 | B、注意实验安全 |
| ①固体二氧化碳-干冰 ②氢氧化钙-熟石灰 ③氢氧化钠-苛性钠 | ①点燃可燃性气体前一定要验纯 ②鉴别化学药品时可以品尝 ③危险实验配戴防护眼镜 |
| C、合理利用资源 | D、健康生活方式 |
| ①随意大量使用塑料袋 ②过量使用农药,提高农作物产量 ③开发新能源 | ①平衡膳食,不偏食挑食 ②不食用过期食品 ③不过量引用碳酸饮料 |
| A. | A | B. | B | C. | C | D. | D |
20.下列物质的用途主要利用其化学性质的是( )
| A. | 稀有气体用来制作电光源 | B. | 天然气用作燃料 | ||
| C. | 干冰用于人工降雨 | D. | 铜用于制造导线 |
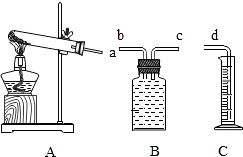
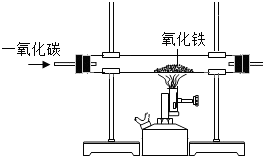 金属材料在生产、生活与科学研究中应用广泛.请根据所学化学知识回答下列问题:
金属材料在生产、生活与科学研究中应用广泛.请根据所学化学知识回答下列问题: 如图所示是某同学为净化浑浊的井水而采用的过滤实验操作图,试回答:
如图所示是某同学为净化浑浊的井水而采用的过滤实验操作图,试回答: