题目内容
9.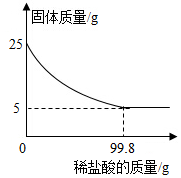 为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:(1)这种贝壳中碳酸钙的质量分数是80%.
(2)25g贝壳与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数.
分析 由图可以看固体减少了20g即碳酸钙的质量为20g,根据碳酸钙的质量和对应的化学方程式求算氯化钙和二氧化碳的质量,进而求算对应的质量分数.
解答 解:由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为$\frac{20g}{25g}$×100%=80%
设恰好反应时,生成氯化钙的质量为x,同时产生二氧化碳的质量为y
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 111 44
20g x y
$\frac{100}{20g}$=$\frac{111}{x}$=$\frac{44}{y}$
x=22.2g
y=8.8g
所得溶液中溶质的质量分数=$\frac{22.2g}{20g+99.8g-8.8g}$×100%=20%
答:(1)这种贝壳中碳酸钙的质量分数是 80%.
(2)25g贝壳与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为20%
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
17.以下事实用微观粒子的知识解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 一畦春韭绿,十里稻花香 | 分子不断运动 |
| B | 水结冰后体积变大 | 水分子体积变大 |
| C | 1滴水中大约有1.67×1021个水分子 | 分子很小 |
| D | 6000L氧气加压后可装入容积为40L的钢瓶中 | 分子间有间隔 |
| A. | A | B. | B | C. | C | D. | D |
14.下列各组物质的分离操作可按溶解、过滤、蒸发溶剂的顺序进行的是( )
| A. | 食盐和蔗糖 | B. | 铜粉和铁粉 | ||
| C. | 水和酒精的混合物 | D. | 食盐和泥沙 |
1.鉴别下列物质的方法(括号内为方法)中不能达到目的是( )
| A. | 硬水和软水(加入肥皂水) | B. | 稀HCl和NaCl溶液(滴入酚酞溶液) | ||
| C. | NH4NO3和KCl固体(熟石灰混合研磨) | D. | 羊毛和涤纶(灼烧) |
18.右表是“部分酸、碱和盐的溶解性表(室温)”中的一部分,下列与“★”处有关的说法正确的是( )
| 阳离子 | 阴离子 | ||
| … | NO3- | Cl- | |
| … | … | … | … |
| Cu2+ | … | ★ | 溶 |
| Ag+ | … | 溶 | 不 |
| A. | ★处对应物质的化学式是CuNO3 | B. | ★对应物质属于盐 | ||
| C. | ★处应填“不” | D. | ★对应物质的溶液为浅绿色 |