题目内容
3.请用所学化学知识解释下列现象:(1)餐具上的油污可以用加洗洁精的水洗掉,说明洗洁精具有乳化作用;
(2)夏天鱼池内需要增氧,是因为温度升高,氧气溶解度减小;
(3)铝的化学性质很活泼,但家里用了很久的铝壶很少出现腐蚀,请用化学方程式表明其中的原理4Al+3O2=2Al2O3;
(4)实验室不用催化剂制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(5)纯净的氢气在空气中燃烧的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
分析 (1)根据洗洁精具有乳化作用解答;
(2)根据气体的溶解度随温度的升高而减小解答;
(3)根据铝具有良好抗腐蚀性的原因进行分析解答;
(4)根据实验室不用催化剂制取氧气的物质是高锰酸钾解答;
(5)氢气在空气中燃烧生成水解答.
解答 解:
(1)餐具上的油污可以用加洗洁精的水洗掉,说明洗洁精具有乳化作用;
(2)夏天鱼池内需要增氧,是因为温度升高,氧气溶解度减小;
(3)铝的化学性质非常活泼,极易和氧气反应生成氧化铝薄膜,阻碍铝的进一步氧化,所以铝制品却很耐腐蚀原因是:铝在常温下与空气中的氧气反应,在其表面形成致密的氧化铝薄膜,阻止铝进一步被氧化,铝和氧气反应生成氧化铝,化学方程式为:4Al+3O2=2Al2O3.
(4)实验室不用催化剂制取氧气的物质是高锰酸钾,化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(5)纯净的氢气在空气中燃烧的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
答案
(1)乳化;
(2)温度升高,氧气溶解度减小
(3)4Al+3O2=2Al2O3
(4)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(5)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.如表中列出了氯化铵在不同温度下的溶解度:
①从表中可知:随温度升高氯化铵的溶解度增大.
②20℃时,向盛有100g水的烧杯中加入50g氯化铵,充分搅拌,则烧杯中溶液的质量为137.2g.将该混合物升温至60℃,观察到的现象是烧杯底部不溶解的氯化铵全部溶解,得到氯化铵的不饱和(填“饱和”或“不饱和“)溶液.
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度(g) | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
②20℃时,向盛有100g水的烧杯中加入50g氯化铵,充分搅拌,则烧杯中溶液的质量为137.2g.将该混合物升温至60℃,观察到的现象是烧杯底部不溶解的氯化铵全部溶解,得到氯化铵的不饱和(填“饱和”或“不饱和“)溶液.
14.下列变化属于物理变化的是( )
| A. | 白醋使紫色石蕊试液变红 | B. | 用干冰进行人工降雨 | ||
| C. | 铁锈溶解在稀盐酸里 | D. | 以粮食为原料酿酒 |
11.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物 质 | 杂 质 | 除杂所用试剂和方法 | |
| A | H2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| B | NaOH溶液 | Ca(OH)2溶液 | 先加入过量的Na2CO3溶液,再过滤 |
| C | CO2气体 | CO气体 | 通过灼热的CuO |
| D | CaO固体 | CaCO3固体 | 加入适量的稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
18.下列实验操作正确的是( )
| A. |  量取液体 | B. |  闻气体气味 | C. |  氢气验纯 | D. |  加热液体 |
15.下列有关二氧化碳的说法正确的是( )
| A. | 二氧化碳是引发酸雨的“罪魁” | B. | 二氧化碳可用于灭火 | ||
| C. | 二氧化碳可使紫色石蕊试液变蓝 | D. | 二氧化碳有毒不能制作碳酸饮料 |
12.住宅和商场等地发生火灾,消防人员用高压水枪喷水灭火.水在灭火中的主要作用是( )
| A. | 降低燃烧物的着火点 | B. | 防止燃烧时产生的物质污染空气 | ||
| C. | 降低温度到着火点以下 | D. | 使燃烧物隔绝空气 |
16.研究和控制化学反应条件有重要意义.
①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的D(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,因此加热不适合用于双氧水制取氧气.
②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
Ⅰ. 取用二氧化锰的仪器是图2中的B(选填编号).
Ⅱ.写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.本实验中收集氧气选用的装置有A、C和D(选填编号).
Ⅳ.实验2中双氧水溶质质量分数为12%.
Ⅴ.实验3中,加入的二氧化锰质量为5g.
Ⅵ.相同条件下,实验3产生氧气的速率最快,说明在相同的条件下,双氧水的溶质质量分数越大,反应速率越快.
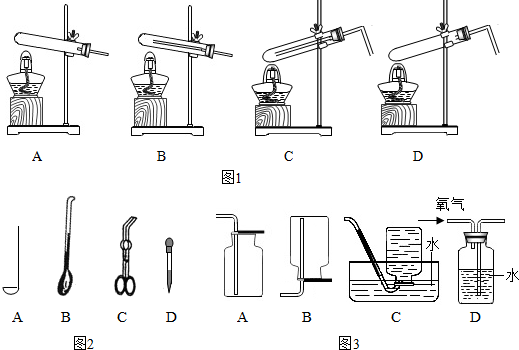
①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的D(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,因此加热不适合用于双氧水制取氧气.
②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
Ⅱ.写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
Ⅲ.本实验中收集氧气选用的装置有A、C和D(选填编号).
Ⅳ.实验2中双氧水溶质质量分数为12%.
Ⅴ.实验3中,加入的二氧化锰质量为5g.
Ⅵ.相同条件下,实验3产生氧气的速率最快,说明在相同的条件下,双氧水的溶质质量分数越大,反应速率越快.

 ;
;