题目内容
下列有关16号元素硫(S)的说法不正确的是( )
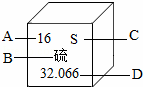
A.该元素原子的质子数为16
B.该元素原子的核电荷数为16
C.该元素原子的核外电子数为16
D.该元素为金属元素
【考点】元素周期表的特点及其应用.
【专题】化学用语和质量守恒定律.
【分析】根据元素周期表中的一个小格所提供的信息,其中原子序数=核电荷数=核外电子数=质子数=16,相对原子质量为32.066,以及元素种类进行解答.
【解答】解:A、根据元素周期表中所提供的硫元素信息可知:质子数为16;故A 正确;
B、根据元素周期表中所提供的硫元素信息可知:核电荷数为16;故B正确;
C、根据元素周期表中所提供的硫元素信息可知:核外电子数为16;故C正确;
D、根据化学元素汉字名称的偏旁可辨别元素的种类,固态非金属元素名称有“石”字旁,可知硫元素属于非金属元素;故D错误.
故选D.
【点评】本题考查学生对元素周期表中知识的理解与掌握,并能在解题中灵活应用的能力.

 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案某化学兴趣小组取用生石灰时,发现装生石灰(CaO)的塑料试剂瓶已经膨胀破裂.他们请教老师后得知该生石灰已经变质.他们对瓶内固体的成分产生了好奇,于是他们对这瓶固体的成分展开了探究.
【提出问题】这瓶久置的生石灰的成分是什么?
【猜想假设】猜想一:全部是Ca(OH)2
猜想二:是CaO和Ca(OH)2的混合物
猜想三:是Ca(OH)2和CaCO3的混合物
你还可以作出的猜想是:
【查阅资料】Ca(OH)2微溶于水,能与稀盐酸反应生成氯化钙和水.
【分析判断】该固体可能含有Ca(OH)2的原因是 (用化学方程式表示)
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体,倒入适量水,充分搅拌、静置 |
| 固体中一定不含CaO |
| ②取上层清液于试管中,通入二氧化碳 | 变浑浊 | 固体中 |
| ③另取少量固体放入试管中,加入稀盐酸 | 有气泡冒出 | 固体中一定含CaCO3 |
写出操作②中发生的化学反应方程式 .
【实验结论】
通过以上实验探究,得出猜想 成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意 .
【数据处理】
为测定该固体中碳酸钙的质量分数,取样品10g于烧杯中加入稀盐酸50g,恰好完全反应,反应后烧杯中物质总质量为56.7g,则该固体中碳酸钙的质量分数是75%(写出具体的计算过程).
某化工厂用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应。实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)

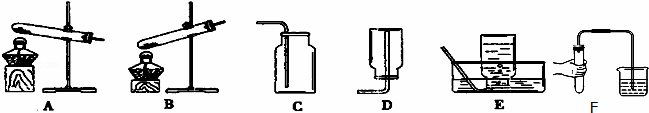
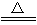 2Fe2O3+4K2O+3O2↑)、遇水将变质(4K2FeO4+10H2O═4Fe(OH)3+8KOH+3O2↑)。根据要求回答下列问题:
2Fe2O3+4K2O+3O2↑)、遇水将变质(4K2FeO4+10H2O═4Fe(OH)3+8KOH+3O2↑)。根据要求回答下列问题: