题目内容
11.同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 80 | 75 | 70 | 66 | 58 | X | 58 |
(1)表中X为58.
(2)当石灰石完全反应后,生成CO2的质量为22g.
(3)求该石灰石中CaCO3的质量分数,写出计算过程.
分析 煅烧石灰石时碳酸钙分解放出二氧化碳而使反应后固体质量减小,直到碳酸钙完全分解,剩余固体质量不再改变;利用质量守恒定律,由反应前后固体质量差计算出反应放出二氧化碳的质量,然后由反应的化学方程式,利用放出二氧化碳的质量求得石灰石样品中所含碳酸钙的质量,从而计算出样品中碳酸钙的质量分数.
解答 解:(1)根据表中数据分析可知t4时,继续煅烧剩余固体质量不再减小,说明碳酸钙已完全分解,故x的值为58;故填:58;
(2)由实验记录数据可知,在反应进行至t4时,继续煅烧剩余固体质量不再减小,说明碳酸钙已完全分解,根据质量守恒定律,生成二氧化碳的质量=80g-58g=22g;故答案为:22;
(3)设80g石灰石中含CaCO3的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 22g
$\frac{100}{x}=\frac{44}{22g}$
x=50g
石灰石中CaCO3的质量分数为:$\frac{50g}{80g}$×100%=62.5%
答:该石灰石中CaCO3的质量分数为62.5%.
点评 利用图表中的数据,结合质量守恒定律分析得到生成二氧化碳的质量,是解决问题的基础,也体现分析问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.下列各组物质,能在pH=1的溶液中大量共存,且形成无色溶液的是( )
| A. | NaNO3 HCl Na2SO4 | B. | NaNO3 NaCl CuSO4 | ||
| C. | NaCl Na2SO4 Na2CO3 | D. | NaOH CaCl2 Na2SO4 |
2.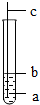 如图,在水里铁丝各部位生锈的速率是不相等的,其关系式正确的是( )
如图,在水里铁丝各部位生锈的速率是不相等的,其关系式正确的是( )
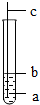 如图,在水里铁丝各部位生锈的速率是不相等的,其关系式正确的是( )
如图,在水里铁丝各部位生锈的速率是不相等的,其关系式正确的是( )| A. | Va>Vb>Vc | B. | Va>Vb=Vc | C. | Va=Vb>Vc | D. | Vb>Va>Vc |
19.下列反应不属于置换反应的是( )
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | D. | Fe+CuSO4═FeSO4+Cu |
16.豆浆被成为“植物奶”,其中含有的异黄酮(C15H10O2)具有防癌功能.关于异黄酮说法正确的是( )
| A. | 异黄酮中共含有27个原子 | |
| B. | 异黄酮中含有C、H、O三种元素 | |
| C. | 异黄酮分子中含有氧分子 | |
| D. | 异黄酮中C、H、O三种元素的质量比为15:10:2 |
1.一块4克的合金,与足量的盐酸反应,产生0.2克氢气,则该合金的组成可能为( )
| A. | Fe Mg | B. | Fe Al | C. | Fe Zn | D. | Al Mg |