题目内容
3.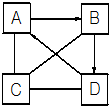 A、B、C、D是初中化学常见的四种不同类别的物质,A、B、D在一定条件下可相互转化,C与A、B、D均能发生反应,D与C发生中和反应,C还能与AgNO3溶液反应可产生不溶于稀硝酸的白色沉淀.(-表示两端的物质间能发生化学反应;→表示物质间存在转化关系;)
A、B、C、D是初中化学常见的四种不同类别的物质,A、B、D在一定条件下可相互转化,C与A、B、D均能发生反应,D与C发生中和反应,C还能与AgNO3溶液反应可产生不溶于稀硝酸的白色沉淀.(-表示两端的物质间能发生化学反应;→表示物质间存在转化关系;)(1)请根据已知条件推断B的化学式为:CaO
(2)请写出D与C的化学方程式:Ca(OH)2+2HCl=CaCl2+2H2O,其基本反应类型是复分解反应.
(3)试列举A的一种重要用途:做建筑材料等.
分析 根据题干提供的信息进行分析解答,D与C发生中和反应,C还能与AgNO3溶液反应可产生不溶于稀硝酸的白色沉淀,因此C是盐酸,则D是碱;A、B、C、D是初中化学常见的四种不同类别的物质,A、B、D在一定条件下可相互转化,C与A、B、D均能发生反应,因此A、B、D应该是碱、盐、氧化物,B-碱能够转化为A,因此可以假设D是氢氧化钙,则A是碳酸钙,B是氧化钙,带入验证完成相关的问题.
解答 解:D与C发生中和反应,C还能与AgNO3溶液反应可产生不溶于稀硝酸的白色沉淀,因此C是盐酸,则D是碱;A、B、C、D是初中化学常见的四种不同类别的物质,A、B、D在一定条件下可相互转化,C与A、B、D均能发生反应,因此A、B、D应该是碱、盐、氧化物,B-碱能够转化为A,因此可以假设D是氢氧化钙,则A是碳酸钙,B是氧化钙,带入验证符合转化关系,因此:
(1)B是氧化钙,故天:CaO;
(2)盐酸和氢氧化钙反应产生氯化钙和水,该反应属于复分解反应;故填:Ca(OH)2+2HCl=CaCl2+2H2O;复分解反应;
(3)碳酸钙可以用于建筑材料等;故填:做建筑材料等.
点评 本题为框图式物质推断题,解答本题的关键是依据题干叙述找准解题的突破口,直接得出有关物质的化学式,然后依据框图推断出其他物质的化学式.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
13.下列实验现象与事实不相符的是( )
| A. | 加热饱和石灰水,出现白色沉淀 | |
| B. | 氨水中滴加几滴石蕊试液,溶液呈蓝色 | |
| C. | 稀硫酸加入少量铁粉,溶液逐渐变成黄色 | |
| D. | 氢氧化钠溶液中滴加硫酸铜溶液,生成蓝色沉淀 |
11.写出相应的元素符号或元素名称
| 符号 | H | He | F | Ne | |||||||
| 名称 | 磷 | 碳 | 氮 | 氧 | 钠 | 镁 | 铝 | ||||
| 符号 | I | ||||||||||
| 名称 | 硫 | 氯 | 钾 | 钙 | 锰 | 铁 | 铜 | 锌 | 银 | 钡 |
18.将一定量的锌粉加入到硫酸亚铁、硫酸铜和硫酸镁的混合溶液中,一段时间后过滤,向滤渣中加入稀盐酸有气泡产生,则下列说法正确的是( )
①滤渣中一定有锌
②滤渣中一定有铜,可能有锌
③向滤渣中加入足量的稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
①滤渣中一定有锌
②滤渣中一定有铜,可能有锌
③向滤渣中加入足量的稀盐酸,最后溶液一定变成浅绿色
④滤液中溶质一定含有硫酸锌和硫酸镁
⑤滤液的颜色不可能为浅绿色.
| A. | ②④ | B. | ①④⑤ | C. | ②③④ | D. | ②③④⑤ |
15.下列有关废金属回收的说法错误的是( )
| A. | 废金属的增多造成资源浪费 | |
| B. | 回收利用废金属可以带来巨大的社会效益和经济效益 | |
| C. | 废金属无需回收,对人类无危害 | |
| D. | 回收废金属可以减少环境污染 |
12. 小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸
小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸
钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,他认为该溶液不可能是氢氧化钙溶液,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断该溶液中不可能是氯化钠.对他的操作方法、测量结果及结论的评价,正确是B.
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(3)为了进一步确定该溶液的成分,小亮继续进行下列实验.
【设计实验方案】方案甲:选择氯化钡溶液来确定该溶液的成分;
方案乙:选择稀盐酸来确定该溶液的成分.
【进行实验】在两个方案中任选一个方案进行实验,填写步骤、现象、结论.
【实验反思】①有同学认为还可以用一种常见的碱溶液来确定是碳酸钠,它是Ca(OH)2溶液.有关反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
②小亮经过反思,向同学们提出如下建议,你认为不合理的是C.(填序号)
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.
 小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸
小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分只能看出溶质质量分数为10%.老师说,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠中的一种.
(1)小亮查阅氢氧化钙常温下的溶解度为0.18g后,他认为该溶液不可能是氢氧化钙溶液,理由是常温下不可能得到质量分数为10%的氢氧化钙溶液.
(2)小亮用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,他判断该溶液中不可能是氯化钠.对他的操作方法、测量结果及结论的评价,正确是B.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加稀硫酸溶液 氯化钡溶液 | 有气泡冒出, 出现白色沉淀 | 该溶液是碳酸钠溶液.反应方程式为: Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ Na2CO3+BaCl2═2NaCl+BaCO3↓. |
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(3)为了进一步确定该溶液的成分,小亮继续进行下列实验.
【设计实验方案】方案甲:选择氯化钡溶液来确定该溶液的成分;
方案乙:选择稀盐酸来确定该溶液的成分.
【进行实验】在两个方案中任选一个方案进行实验,填写步骤、现象、结论.
【实验反思】①有同学认为还可以用一种常见的碱溶液来确定是碳酸钠,它是Ca(OH)2溶液.有关反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
②小亮经过反思,向同学们提出如下建议,你认为不合理的是C.(填序号)
A.倾倒液体时应注意保护标签不被腐蚀
B.要有严谨的科学实验的态度
C.无法辨认的药品,直接倒掉,无需保留.