题目内容
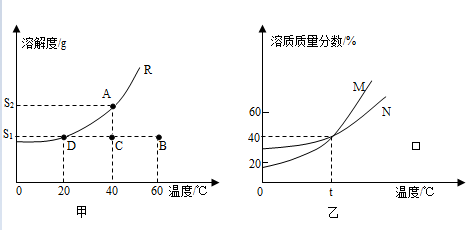
如图1是甲、乙两种物质的溶解度曲线,请回答下列问题.

(1) ℃时,甲、乙两种物质的溶解度相等.
(2)将乙的饱和溶液变成不饱和溶液的方法是 (任写一种).
(3)小明同学用甲物质进行以下实验(如图2):
①实验过程中,所得溶液溶质质量分数相同的是 (填字母序号).
②向B中溶液再加入60g甲固体的过程中,发现先固体全部溶解,一段时间后又有部分固体析出.你认为“全部溶解”的原因是 .

(1)
(2)将乙的饱和溶液变成不饱和溶液的方法是
(3)小明同学用甲物质进行以下实验(如图2):
①实验过程中,所得溶液溶质质量分数相同的是
②向B中溶液再加入60g甲固体的过程中,发现先固体全部溶解,一段时间后又有部分固体析出.你认为“全部溶解”的原因是
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:根据固体的溶解度曲线可以:①比较不同物质在同一温度下的溶解度大小,②判断出物质的溶解度随温度变化的变化情况.根据t1℃时甲的溶解度等于65g,可知该温度下100g水中做多溶解65g该物质,所以B能溶得到的是不饱和溶液;再加入60g甲不能全部溶解,溶解了65g,所以C饱和;升温到t2℃时甲的溶解度为90g,说明100g水中在此温度下可溶解90克甲,加了100g甲物质,所得溶液D为饱和溶液;降温到t1℃时,溶解度降低所得溶液E饱和,溶解了65g,综上分析解答
解答:解:(1)据图可以看出,在t1℃时,甲、乙两种物质的溶解度相等,故填:t1;
(2)乙的溶解度随温度的升高而减小,要将乙的饱和溶液变成不饱和溶液可以采用加水或降低温度的方法,故填:加水或降低温度;
(3)①根据t1℃时甲的溶解度等于65g,可知该温度下100g水中做多溶解65g该物质,所以B能溶得到的是不饱和溶液;再加入60g甲不能全部溶解,溶解了65g,所以C饱和;升温到t2℃时甲的溶解度为90g,说明100g水中在此温度下可溶解90克甲,加了100g甲物质,所得溶液D为饱和溶液;降温到t1℃时,溶解度降低所得溶液E饱和,溶解了65g,根据饱和溶液的溶质质量分数
×100%,E溶液与C溶液中溶质的质量分数相同,故填:CE;
②向B中溶液再加入60g甲固体的过程中,发现先固体全部溶解,一段时间后又有部分固体析出,原因是甲溶于水放热,使溶液温度升高,甲的溶解度增大,故填:甲溶于水放热,使溶液温度升高,甲的溶解度增大.
(2)乙的溶解度随温度的升高而减小,要将乙的饱和溶液变成不饱和溶液可以采用加水或降低温度的方法,故填:加水或降低温度;
(3)①根据t1℃时甲的溶解度等于65g,可知该温度下100g水中做多溶解65g该物质,所以B能溶得到的是不饱和溶液;再加入60g甲不能全部溶解,溶解了65g,所以C饱和;升温到t2℃时甲的溶解度为90g,说明100g水中在此温度下可溶解90克甲,加了100g甲物质,所得溶液D为饱和溶液;降温到t1℃时,溶解度降低所得溶液E饱和,溶解了65g,根据饱和溶液的溶质质量分数
| 溶解度 |
| 溶解度+100g |
②向B中溶液再加入60g甲固体的过程中,发现先固体全部溶解,一段时间后又有部分固体析出,原因是甲溶于水放热,使溶液温度升高,甲的溶解度增大,故填:甲溶于水放热,使溶液温度升高,甲的溶解度增大.
点评:本题难度不大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题.

练习册系列答案
相关题目
下列化学实验操作中,不正确的是( )
| A、用灯帽盖灭酒精灯的火焰 |
| B、稀释浓硫酸时,将浓硫酸缓缓加到水中,并不断用玻璃棒搅拌 |
| C、将固体氢氧化钠直接放在托盘天平上称量 |
| D、给试管里的固体加热,试管口应稍稍向下倾斜 |
| E、被雨淋湿的自行车应立即擦干以防生锈 |
| F、用氢氧化钠溶液清除餐具上的油污 |
我国已研究出新型水处理剂ClO2的新制法,其反应的微观过程如图所示.下列说法正确的是( )
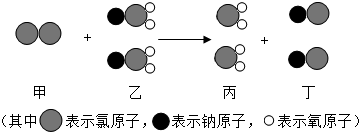

| A、乙中氯元素的化合价为+5价 |
| B、该反应属于复分解反应 |
| C、该反应中分子的数目和种类都改变了 |
| D、该反应的化学方程式为2Cl+NaClO2═2ClO2+2NaCl |
下列应用在高铁列车上的材料,不属于金属材料的是( )
| A、特种钢 | B、玻璃 |
| C、铝合金 | D、铜线 |