题目内容
20. 水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列问题:
水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列问题:(1)下列是一些净水的方法,其中可使硬水变成软水的是③④(填序号).
①沉淀 ②过滤 ③煮沸 ④蒸馏
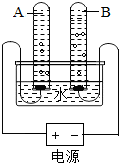
(2)按如图所示装置进行实验,一段时间后,理论上B试管中产生的气体与A试管中产生的气体的体积比为2:1,该实验过程中发生反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)请举出你在生活中节约用水的一种做法洗菜水浇花(或洗衣服水拖地、冲厕所或使用节水龙头等).
分析 (1)根据使硬水变成软水的方法有蒸馏和煮沸进行解答;
(2)根据电解水生成氢气和氧气进行解答;
(3)根据生活中节约用水的措施进行解答.
解答 解:(1)使硬水变成软水的方法有蒸馏和煮沸,而过滤、沉淀只除掉水中难溶性杂质;
故填:③④;
(2)电解水生成氢气和氧气,负极产生氢气,正极产生氧气,二者的体积比为2:1;该反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
故填:2:1;2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)生活中节约用水的措施有洗菜水浇花(或洗衣服水拖地、冲厕所或使用节水龙头等);
故填:洗菜水浇花(或洗衣服水拖地、冲厕所或使用节水龙头等).
点评 本题难度不大,了解净化水的常用方法、硬水与软水的转化方法、电解水生成氢气和氧气等是正确解答本题的关键.

练习册系列答案
相关题目
10.下列物质的主要成分与化学式相符合的是( )
| A. | 纯碱 NaOH | B. | 天然气 CH4 | C. | 生石灰 Ca(OH)2 | D. | 苏打 NaHCO3 |
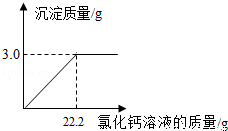
8.分析处理图表中的信息是学习化学的一种重要方法. 如表是氯化钠和硝酸钾在不同温度时的溶解度,仔细阅读并回答下列问题.
(1)上述两种物质中,NaCl(填化学式)的溶解度受温度影响较小.
(2)在40℃时,将40g硝酸钾固体加入到100g水中,搅拌充分后得到是不饱和溶液(填“饱和”或“不饱和”).
(3)针对上述信息,甲、乙、丙三位同学分别得到如下结论,你认为说法正确的是乙.
甲:KNO3饱和溶液中一定不能再溶解NaCl固体.
乙:KNO3与NaCl溶解度相等时的温度一定在20℃-40℃之间.
丙:40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大.
| 温度/℃ | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | |
(2)在40℃时,将40g硝酸钾固体加入到100g水中,搅拌充分后得到是不饱和溶液(填“饱和”或“不饱和”).
(3)针对上述信息,甲、乙、丙三位同学分别得到如下结论,你认为说法正确的是乙.
甲:KNO3饱和溶液中一定不能再溶解NaCl固体.
乙:KNO3与NaCl溶解度相等时的温度一定在20℃-40℃之间.
丙:40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大.
15.下列四种粒子的结构示意图中,表示阳离子的是( )
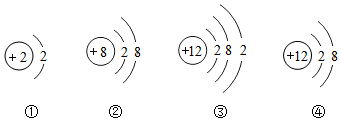

| A. | ① | B. | ② | C. | ③ | D. | ④ |
5.某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把40g稀盐酸(氯化氢的水溶液)分四次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水)充分反应后经过过滤、干燥等操作,最后称量,得实验数据如表:
(1)是护士样品中碳酸钙的质量分数为85%.
(2)求所用稀盐酸的溶质质量分数?
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入10g | 3.0g |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.0g |
| 第四次加入10g | 0.6g |
(2)求所用稀盐酸的溶质质量分数?