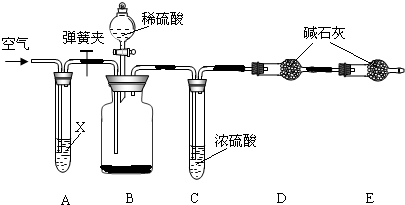
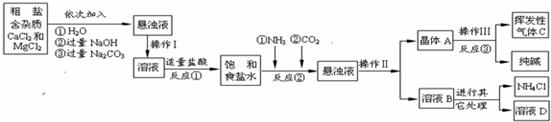
题目内容
“侯氏制碱法”制得的纯碱中含有少量氯化钠.取NaCl和Na2CO3的固体混合物25克溶于适量的蒸馏水中,滴入稀盐酸至恰好完全反应,得到10%的NaCl溶液272克.
(化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑)
求:(1)反应后所得溶液中溶质的质量.
(2)原固体混合物中NaCl的质量分数.
| (1)溶质的质量=溶液的质量×溶质的质量分数; (2)原混合物的质量是25g,而反应后固体的质量﹣﹣氯化钠为27.2g,固体质量增加是因为碳酸钠和盐酸反应变为氯化钠,可据差量法计算混合物中Na2CO3的质量,进而计算出混合物中氯化钠的质量及其质量分数. | |
| 解答: | 解:(1)反应后所得溶液中NaCl的质量为272g×10%=27.2g; (2)原混合物的质量是25g,而反应后固体的质量﹣﹣氯化钠为27.2g,固体质量增加是因为碳酸钠和盐酸反应变为氯化钠,可据差量法计算, 设原固体混合物中Na2CO3的质量为x Na2CO3+2HCl═2NaCl+H2O+CO2↑ 固体质量增加 106 117 117﹣106=11 x 27.2g﹣25g=2.2g
x=21.2g 所以原固体混合物中NaCl的质量为:25g﹣21.2g=3.8g 则混合物中NaCl的质量分数为 答:反应后所得溶液中溶质的质量是27.2g; 原固体混合物中NaCl的质量分数是15.2%. |

练习册系列答案
相关题目
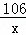 =
=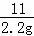
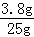 ×100%=15.2%
×100%=15.2%