题目内容
4.从微观视角看物质的变化是化学研究的内容之一.下图分别表示生成氯化钠的不同化学反应.请根据图示回答相关问题: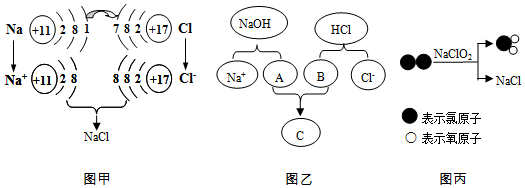
(1)由图甲可知,反应中得到电子的是氯原子;钠元素在元素周期表中的位置位于第三周期.
(2)由图乙可知,NaOH溶液与盐酸反应的微观实质是氢离子与氢氧根离子结合生成水分子.
(3)图丙表示反应的化学方程式为Cl2+2NaClO2=2ClO2+2NaCl;NaClO2中氯的化合价是+3.
(4)由图可知氯化钠是由离子(填“离子”、“分子”、“原子”)构成;锶元素(元素符号为Sr)的原子最外层电子数为2,则氯化锶的化学式为SrCl2 .
分析 (1)依据反应中原子的核外电子变化情况分析解答;
(2)根据中和反应的实质进行判断即可;
(3)根据氧化物和微观示意图中相关分子的结构书写相关的化学式;
(4)根据物质的微粒构成进行分析解答;根据化学式的写法解答.
解答 解:
(1)依据金属钠与氯气反应生成氯化钠的微观示意图可知,该变化过程中两种原子的最外层电子数都发生了变化,反应中得到电子的是氯原子,钠元素的原子核外有3个电子层,在元素周期表中的位置位于第三周期;
(2)依据氢氧化钠能够电离出钠离子和氢氧根离子,盐酸能够电离出氢离子和氯离子,由图乙可知,NaOH溶液与盐酸反应的微观实质是氢离子与氢氧根离子结合生成水分子;
(3)由图示中分子的微观结构可知该反应的反应物是Cl2和NaClO2,生成物是ClO2和NaCl,所以该反应的方程式为:Cl2+2NaClO2=2ClO2+2NaCl.
根据化合价原则,NaClO2中钠元素和氧元素的化合价依次为+1价和-2价,故氯元素的化合价为:+1+x+(-2)×2═0,故x=+3.
(4)由图可知氯化钠是由离子构成;锶元素(元素符号为Sr)的原子最外层电子数为2,易失去2个电子,化合价为+2价,氯元素为-价,则氯化锶的化学式为SrCl2.
故答案为:
(1)氯原子; 三;
(2)氢离子与氢氧根离子结合生成水分子;
(3)Cl2+2NaClO2=2ClO2+2NaCl;+3;
(4)离子; SrCl2
点评 根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成,是解答本题的基本方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.关于化学反应A+B=C+D,下列说法中正确的是( )
| A. | 若生成物C和D分别是盐和水,则反应物一定是酸和碱 | |
| B. | 若C是单质、D为化合物,则该反应一定是置换反应 | |
| C. | 若A.B各取10g混合,使其充分反应,则C,D质量的总和一定等于20g | |
| D. | 若B是酸,则C和D一定有一种是盐 |
19.下列认识中,正确的是( )
| A. | 合金、塑料、橡胶都属于合成材料 | |
| B. | 催化剂在化学反应前后质量不变 | |
| C. | 饱和溶液一定比不饱和溶液的浓度大 | |
| D. | 用汽油洗涤油污原理属于乳化作用 |
9.“苯宝宝”家族中的苯酚( )是一种具有特殊气味的无色针状晶体,它是生产常用药--阿司匹林的重要原料.下列关于苯酚的说法正确的是( )
)是一种具有特殊气味的无色针状晶体,它是生产常用药--阿司匹林的重要原料.下列关于苯酚的说法正确的是( )
 )是一种具有特殊气味的无色针状晶体,它是生产常用药--阿司匹林的重要原料.下列关于苯酚的说法正确的是( )
)是一种具有特殊气味的无色针状晶体,它是生产常用药--阿司匹林的重要原料.下列关于苯酚的说法正确的是( )| A. | 苯酚是一种氧化物 | B. | 苯酚中氧元素的质量分数最小 | ||
| C. | 一个苯酚分子由13个原子构成 | D. | 苯酚中碳、氢元素质量比为1:1 |
14. 如图所示的实验装置可用来测定某气体X的组成.在注射器A中装有0.32g气体X并慢慢通过不含空气并装有足量灼热的氧化铜的玻璃管B,使气体X完全反应.得到以下实验结果:实验前B管重20.32克,实验后B管重20.00克,B管中出现红色粉末.C管中收集到的无色液体是水;注射器D中收集到生成的氮气0.28克.下列说法正确的是( )
如图所示的实验装置可用来测定某气体X的组成.在注射器A中装有0.32g气体X并慢慢通过不含空气并装有足量灼热的氧化铜的玻璃管B,使气体X完全反应.得到以下实验结果:实验前B管重20.32克,实验后B管重20.00克,B管中出现红色粉末.C管中收集到的无色液体是水;注射器D中收集到生成的氮气0.28克.下列说法正确的是( )
 如图所示的实验装置可用来测定某气体X的组成.在注射器A中装有0.32g气体X并慢慢通过不含空气并装有足量灼热的氧化铜的玻璃管B,使气体X完全反应.得到以下实验结果:实验前B管重20.32克,实验后B管重20.00克,B管中出现红色粉末.C管中收集到的无色液体是水;注射器D中收集到生成的氮气0.28克.下列说法正确的是( )
如图所示的实验装置可用来测定某气体X的组成.在注射器A中装有0.32g气体X并慢慢通过不含空气并装有足量灼热的氧化铜的玻璃管B,使气体X完全反应.得到以下实验结果:实验前B管重20.32克,实验后B管重20.00克,B管中出现红色粉末.C管中收集到的无色液体是水;注射器D中收集到生成的氮气0.28克.下列说法正确的是( )| A. | B管中发生的反应为置换反应 | |
| B. | 气体X是氨气(NH3) | |
| C. | 该反应中生成的水与氮气的分子个数比为1:2 | |
| D. | 气体X中氮元素与氢元素的质量比为7:1 |
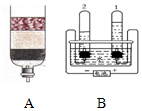 图A为简易净水器的示意图,其中活性炭的作用是吸附异味和色素.图B为电解水的示意图,正极和负极产生气体的体积比为1:2.
图A为简易净水器的示意图,其中活性炭的作用是吸附异味和色素.图B为电解水的示意图,正极和负极产生气体的体积比为1:2.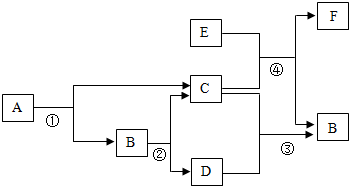 A~F是初中化学常见的物质,它们的相互转化关系如图9所示.已知A、B组成相同,B是人体含量最多的物质,E是最简单的有机物.
A~F是初中化学常见的物质,它们的相互转化关系如图9所示.已知A、B组成相同,B是人体含量最多的物质,E是最简单的有机物.