题目内容
用“侯氏联合制碱法”制得的纯碱常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的含量,小明称取该纯碱样品3.3g,充分溶解于水中,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求:
(1)该纯碱样品中碳酸钠的质量分数.(精确到0.1%)
(2)所加入氯化钙溶液的溶质质量分数.

【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【专题】压轴实验题;利用图像,进行分析计算;有关化学方程式的计算.
【分析】(1)欲求该纯碱样品中碳酸钠的质量分数,须先根据化学方程式求出样品中碳酸钠的质量,再利用质量分数公式计算即可.
(2)欲求所加入氯化钙溶液的溶质质量分数,须先根据化学方程式求出溶质的质量,再根据溶质质量分数= ×100%计算即可.
×100%计算即可.
【解答】解:设该纯碱样品中碳酸钠的质量为x,22.2g氯化钙溶液中溶质的质量为y,则
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111 100
x y 3.0g

解之得:x=3.18g,y=3.33g
所以,该纯碱样品中碳酸钠的质量分数为: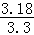 ×100%=96.4%
×100%=96.4%
所加入氯化钙溶液的溶质质量分数为: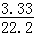 ×100%=15%
×100%=15%
答:该纯碱样品中碳酸钠的质量分数为96.4%,所加入氯化钙溶液的溶质质量分数为15%.
【点评】本题主要考查学生对物质质量分数和溶质质量分数的计算能力.学生需正确书写出化学方程式,然后根据 化
化 学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.
学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.

练习册系列答案
相关题目
 B.
B. C.
C. D.
D.

