题目内容
20.某元素的原子结构示意图如图甲(1)该原子的核电荷数为17,核外有3个电子层.
(2)它的最外层电子数x=7.
(3)该元素属于非金属元素(填“金属元素”、“非金属元素”或“稀有气体元素”).
(4)该原子在化学反应中易得(填“得”或“失”1个电子,变成带1个单位负(填“正”或“负”)电荷的阴(填“阴”或“阳”)离子,该离子的符号为Cl-.
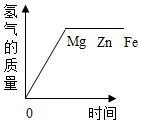
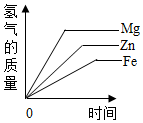
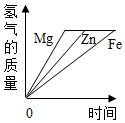
(5)如图乙表示的元素与该元素具有相似化学性质的是C

分析 (1)原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层;
(2)原子结构示意图中,弧线上的数字表示该层上的电子数,核内质子数=核外电子数;
(3)金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有“气”字头,据此进行解答即可;
(4)原子最外层电子数大于4,易得到电子,形成带负电荷的阴离子,离子带的电荷数与原子得失电子的数目相等,据此进行分析解答;
(5)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似.
解答 解:(1)由原子的结构示意图可知,该原子的核电荷数是17,核外有3个电子层;
(2)由核内质子数=核外电子数可知,最外电子层的电子数为17-10=7;
(3)由图甲可知:该元素是氯元素,带“气”字旁,属于非金属元素;
(4)氯原子最外层电子数为7,在化学反应中易得到1个电子,形成带1个单位负电荷的氯离子,是阴离子,其离子符号为:Cl-;
(5)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,则图乙中C与该 元素的化学性质相似;
故答案为:(1)17;3;(2)7;(3)非金属元素;(4)得;1;1;负;阴;Cl-;(5)C.
点评 本题难度不大,灵活运用元素周期表中元素的信息、原子结构示意图的含义是正确解答本题的关键.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
11.下列叙述完全符合质量守恒定律的是( )
| A. | 水结成冰,变化前后质量保持不变 | |
| B. | 50mL水和50mL酒精混合后,体积小于100mL | |
| C. | 10g蔗糖溶解在90g水中,得到100g糖水 | |
| D. | 1.2g碳与3.2g氧气恰好完全反应,可生成4.4g二氧化碳 |
12.下列化学方程式书写正确的是( )
| A. | 加热氯酸钾和二氧化锰的混合物 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | |
| B. | 红磷在氧气中燃烧 P+O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 | |
| C. | 铁丝在氧气中燃烧 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | |
| D. | 电解水 2H2O═2H2↑+O2↑ |
9.日常生活中,下列做法错误的是( )
| A. | 生活中用明矾净水 | |
| B. | 用碳素墨水书写比蓝色笔书写的字迹不容易褪色 | |
| C. | 用蒸馏降低水的硬度 | |
| D. | 使用清洁能源能减缓温室效应 |