题目内容
11.已知:将10g氯酸钾和2g二氧化锰混合后放入试管中加热,收集所需要的氧气后,停止加热让试管冷却,称得试管内剩余固体的质量为7.2g,求生成氯化钾的质量.(1)小意很快得到(10g+2g-7.2g)是O2(填化学式)的质量;
(2)进而求出KCl的质量,请你写出小意计算KCl的质量的过程;
(3)小思依据上述计算的结果发现题目数据有问题.请你通过简单的计算,论证他的发现.
(4)如何才能更正该题呢?小意和小思认为有许多方法,例如将题目中“10g氯酸钾”改为“ag氯酸钾”,其他物质的质量不变,则a的取值范围为多少?
分析 (1)①根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.因为化学反应中生成的气体逸出,故生成氧气的质量=参加反应前各物质的质量总和-反应后生成各物质的质量总和;
(2)根据氯酸钾分解的化学方程式和生成氧气的质量,列出比例式,就可计算出生成氯化钾的质量;
(3)剩余固体的质量=生成氯化钾的质量+二氧化锰的质量(催化剂不参与反应);
(4)①根据完全反应后剩余固体的质量和化学方程式计算,得出氯酸钾的质量;
②假设氯酸钾没有反应,也就是氯酸钾最少的质量就是剩余固体质量-二氧化锰质量.
解答 解:(1)①生成氧气的质量为:10g+2g-7.2g=4.8g;
(2)设生成氯化钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 4.8g
$\frac{149}{x}=\frac{96}{4.8g}$
解得:x=7.45g;
(3)所剩固体的质量=7.45g+2g=9.45g>7.2g,所以题目有错误.
(或氯酸钾质量=7.45g+4.8g=12.25g>10g所以题目有错误.)
(4)①如果完全反应后剩余固体质量为7.2g,则氯酸钾质量为y,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 149
y 7.2g-2g
$\frac{245}{y}=\frac{149}{7.2g-2g}$
解之得:y=8.55g;
②假设氯酸钾没有完全反应,则其质量为:7.2g-2g=5.2g.
由于氯酸钾一定会分解,只是分解完全与否的问题,所以氯酸钾质量一定大于5.2g.故a的取值范围是:5.2g<a≤8.55g.
故答案为:5.2g<a≤8.55g.
故答案为:
(1)O2,
(2)7.45克;
(3)所剩固体的质量=7.45g+2g=9.45g>7.2g,所以题目有错误.
(4)5.2g<a≤8.55g.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

| A. | 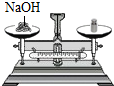 称量NaOH固体 | B. | 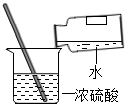 稀释浓硫酸 | C. | 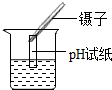 测定溶液的pH | D. |  闻药品的气味 |
①丁烷是由碳、氢两种元素组成的
②丁烷由丁烷分子构成
③丁烷分子由碳、氢两种元素构成
④一个丁烷是由4个碳原子和10个氢原子构成的
⑤丁烷分子是由碳原子和氧原子构成的.
| A. | ①②③④⑤ | B. | ①②④ | C. | ②③④⑤ | D. | ①②⑤ |
| A. | 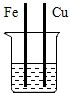 ZnSO4溶液 | B. | 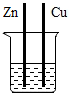 FeSO4溶液 | ||
| C. |  ZnSO4溶液或CuSO4溶液 | D. | 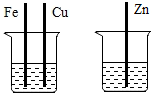 稀盐酸 FeSO4溶液 |
| A. |  稀释浓硫酸 | B. | 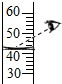 读取液体体积 | ||
| C. | 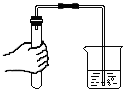 检查装置的气密性 | D. | 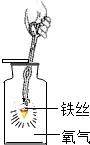 铁丝在氧气中燃烧 |
| A. | 脂肪 | B. | 蛋白质 | C. | 甲烷 | D. | 石灰石 |
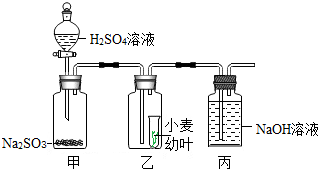 最近几年,频繁的雾霾天气引起大家的重视,雾霾天气是一种大气污染状态,是对大气中各种悬浮颗粒物含量超标的笼统表述,雾霾的有害成分主要来自汽车、工厂、家庭燃烧煤、石油等化石能源产生的二氧化硫、氮氧化物和直径小于2.5微米的可吸入颗粒物,其危害非常大.其中二氧化硫不仅是造成雾霾的元凶,而且还会造成局部地区的酸雨,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠反应可产生SO2气体,设计实验如图所示.
最近几年,频繁的雾霾天气引起大家的重视,雾霾天气是一种大气污染状态,是对大气中各种悬浮颗粒物含量超标的笼统表述,雾霾的有害成分主要来自汽车、工厂、家庭燃烧煤、石油等化石能源产生的二氧化硫、氮氧化物和直径小于2.5微米的可吸入颗粒物,其危害非常大.其中二氧化硫不仅是造成雾霾的元凶,而且还会造成局部地区的酸雨,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠反应可产生SO2气体,设计实验如图所示.