题目内容
1.某化学研究性学习小组在做“寻找新的催化剂”课题时,发现将生锈的铁钉放到过氧化氢溶液中,也可以加快过氧化氢的分解速率.于是,他们对此展开探究:【提出问题】什么物质是该反应催化剂?
【猜想与假设】:下面是组内两位同学所作的猜想,请你完成小华的猜想.
小芳同学:铁钉表面的铁锈(氧化铁)是过氧化氢溶液分解反应的催化剂.
小华同学:铁钉里的铁是过氧化氢溶液分解反应的催化剂.
【实验与结论】
| 实验操作 | 实验现象 | 实验结论 |
| 实验I:把一定质量的氧化铁粉末加入到装有10mL5%的过氧化氢溶液的试管中,并用一根带火星的小木条置于试管口,观察现象. | 产生大量的气泡,带火星的木条复燃 | 反应的符号表达式为:2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑假设一成立 |
| 实验Ⅱ:取10mL5%的过氧化氢溶液于另一支试管中,加入用砂纸打磨光亮的铁钉(或适量铁粉),并用一根带火星的小木条置于试管口,观察现象. | 无现象 | 假设二不成立(填“成立”或“不成立”) |
请你设计实验(写出实验步骤、实验现象及结论)证明其中的某一点理由:
| 实验操作 | 实验现象 | 实验结论 |
分析 此题涉及到“寻找新的催化剂”,将生锈的铁钉放到过氧化氢溶液中探究过氧化氢溶液的分解速率,通过(1)步提出的问题再利用(2)步的猜想与假设,经过(3)步的实验过程及现象得出结论,再经过(4)步的讨论交流,知氧化铁能做过氧化氢溶液的催化剂,而铁单质不能做其反应的催化剂.
解答 解:【猜想与假设】生锈铁钉的组成主要是:氧化铁和铁,假设一:小芳同学:铁钉表面的“氧化铁”是H2O2溶液分解反应的催化剂;假设二:小华同学:铁钉里的“铁”是H2O2溶液分解反应的催化剂;故填:铁;
【实验与结论】】
实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ:把一定质量的氧化铁粉末加入到装有10 mL5%的过氧化氢溶液的试管中,并用一根带火星的小木条置于试管口,观察现象. | 产生大量的气泡,带火星的木条复燃 | 反应的符号表达式为: 2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑ 假设一成立 |
| 实验Ⅱ:取10 mL5%的过氧化氢溶液于另一支试管中,加入用砂纸打磨光亮的铁钉(或适量铁粉),并用一根带火星的小木条置于试管口,观察现象. | 无现象 | 假设二不成立. |
【讨论交流】同学们讨论后认为,小芳的“实验I”还不能够确切的说明氧化铁就是过氧化氢分解制取氧气的催化剂,理由是:还要验证氧化铁的质量和化学性质反应前后是否改变.故填:该实验只验证了氧化铁改变了过氧化氢分解的速率,并未验证其在反应前后的质量和化学性质未发生改变(合理即可);
可设计实验探究氧化铁的化学性质是否发生改变,即对过氧化氢的分解是否仍然具有催化作用,设计如下:实验操作:待实验I反应结束后,在向其中加入适量5%的过氧化氢溶液,将带火星的木条伸入试管口,观察现象;
实验现象:产生大量的气泡,带火星的木条复燃.
实验结论:氧化铁在化学反应前后化学性质未发生改变.
故答案为:
| 实验操作 | 实验现象 | 实验结论 |
| 待实验I反应结束后,在向其中加入适量5%的过氧化氢溶液,将带火星的木条伸入试管口,观察现象. | 产生大量的气泡,带火星的木条复燃. | 氧化铁在化学反应前后化学性质未发生改变 |
点评 本题的思路很明确,就是验证氧化铁对过氧化氢分解是否有催化作用,按照探究实验的步骤按部就班的完成.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
11.下列反应既是氧化反应又是化合反应的是( )
| A. | 石蜡+氢气$\stackrel{点燃}{→}$水+二氧化碳 | B. | 二氧化碳+水→碳酸 | ||
| C. | 铜+氧气$\stackrel{加热}{→}$氧化铜 | D. | 氢气+氧气$\stackrel{点燃}{→}$水 |
12.下列符号既可表示1个原子,又可表示一种元素的是( )
| A. | H | B. | 2N | C. | Na+ | D. | O2 |
9.下列结构示意图中表示阴离子的是( )
| A. | 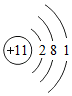 | B. | 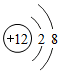 | C. | 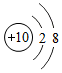 | D. | 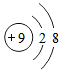 |
11.下列说法正确的是( )
| A. | Fe可以表示一种元素、一个原子和一种物质 | |
| B. | 分子的质量一定比原子的大 | |
| C. | 由一种元素组成的物质是单质 | |
| D. | 水有自净能力,工厂污水不必进行处理即可直接排放 |
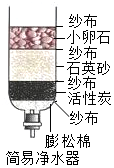 小明假期住在山区的姥姥家,由于山区条件有限,姥姥家一直使用土井取水.每次姥姥从土井里打出水后,都要向水里洒一些白色粉末,小明非常奇怪,于是就对土井水和这些粉末进行了如下探究.
小明假期住在山区的姥姥家,由于山区条件有限,姥姥家一直使用土井取水.每次姥姥从土井里打出水后,都要向水里洒一些白色粉末,小明非常奇怪,于是就对土井水和这些粉末进行了如下探究.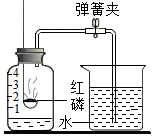 测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内红磷后,立即伸入瓶中并把塞子塞紧.
测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内红磷后,立即伸入瓶中并把塞子塞紧.