题目内容
7.有一种铜的氧化物,其中铜与氧的质量比为8:1,此氧化物中铜元素的化合价为+1.分析 要计算铜的氧化物中铜元素的化合价,首先要确定铜的氧化物的化学式,而确定物质的化学式需要确定分子中的硫原子和氧原子个数;利用原子个数比=$\frac{元素质量比}{相对原子质量比}$可确定原子个数比,从而写出化学式,然后根据化合物中各元素的化合价代数和为0,计算铜元素的化合价.
解答 解:铜的氧化物中硫和氧的原子个数比=$\frac{8}{64}$:$\frac{1}{16}$=2:1,则铜的氧化物的化学式可表示为Cu2O;
氧元素显-2,设铜元素的化合价是x,根据在化合物中正负化合价代数和为零,可知2x+(-2)=0,则x=+1.
故填:+1.
点评 本题是化学式的推断与化合价的计算相结合的综合题,由元素的质量比进行化学式的推断是计算化合价的基础和关键.

练习册系列答案
相关题目
15.下列实验中的做法错误的是( )
| A. | 用红磷燃烧测定空气中氧气的含量时,用足量的红磷 | |
| B. | 做铁丝在氧气中燃烧实验前,在集气瓶内铺一层细沙 | |
| C. | 排水法收集气体,当导管口刚有气泡冒出时立即收集 | |
| D. | 剩余的药品放回原试剂瓶中,不能随意丢弃 |
12.下列实验现象的描述错误的是( )
| A. | 氢气燃烧产生淡蓝色火焰 | |
| B. | 磷在空气中燃烧产生大量的白烟 | |
| C. | 硫在氧气中燃烧发出明亮的蓝紫色火焰,生成带刺激性气味的气体 | |
| D. | 蜡烛在空气中燃烧生成二氧化碳和水 |
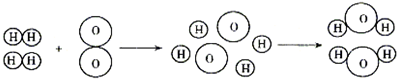
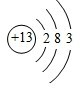 .
. 和
和 构成的化合物Na2O.
构成的化合物Na2O. 下面是几种实验室制取气体的发生装置与收集装置.
下面是几种实验室制取气体的发生装置与收集装置.