��Ŀ����
2�����������DZ���������Դ��һ����Ч;����ij��ҵ���Ϻ�����ͭ��������������һϵ�д�����ɵõ�ͭ������������Һ����Ҫ������ͼ��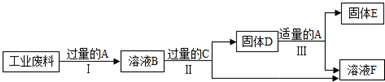
����֪��Fe+Fe2��SO4��3�T3FeSO4 ��
��1�����̢����������ܽ�Ļ�ѧ����ʽ��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
��2�����̢���������C�Ļ�ѧʽ��Fe����������������ѧ��Ӧ�����̢��ַ�Ӧ��Ӧ���е�ʵ������ǹ��ˣ�
��3�����̢��������A������Ӧ�Ļ�ѧ����ʽ��Fe+H2SO4=FeSO4+H2����
��4��A��F�У�������ͭ����Ԫ�ص���BD������ĸ��ţ���
���� �������������ᷴӦ������������ˮ�����벻���Թ����Һ��ʹ�ù��˵ķ�������Ͻ���������εĻ�ѧ���ʽ��н��
��� �⣺��1��Ҫ���յõ��������������ܽ�����ͭ��������ʹ�õ�����ϡ���ᣬ����������ϡ���ᷴӦ������������ˮ�����Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
��2����Ϊ���̢����������ǹ����ģ�������ҺB�к������ᡢ����ͭ����������Ҫ�õ�ͭ����������������Ҫ������������ۣ��������·�Ӧ���������ᷴӦ����������������������������ͭ��Ӧ��������������ͭ��������������Ӧ����������������Ӧ��õ��˹��壨ʣ������ۺ����ɵ�ͭ����Һ�壨����������Һ��������ķ����ǹ��ˣ����Fe���������ˣ�
��3��Ϊ�˽�����ͭ�е�ͭȫ���û���������Ҫ�������������Ҫ�õ���ͭ����Ҫ�������Ὣ����������ȥ���������ᷴӦ�����������������������Fe+H2SO4=FeSO4+H2����
��4�����ݷ����ƶϣ�A�к������ᣬB�к������ᡢ����ͭ����������C������D�к�������ͭ�Ļ���E��ͭ��F�к����������������BD��
���� �����ѶȲ������������Ҫ����ͼ������������Ļ�ѧ���ʡ������Ļ�ѧ���ʵȲ��������������ȷ�����Ĺؼ���

| A�� | ��ˮ��ȥ�������е�̼��� | |
| B�� | ���Ȼ�����ȥ�����л��е�ϡ���� | |
| C�� | ��п����ȥ���������е�����ͭ | |
| D�� | ������������ȥ̼�����л��е������� |
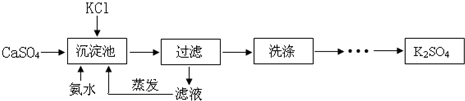
���Ʊ�KClO3��������ͼ1��ʾ��

��֪���ٷ�Ӧ1Ϊ��6Cl2+6Ca��OH��2�TCa��ClO3��2+5CaCl2+6H2O��
���й������ڳ����µ��ܽ�������
| ���� | Ca��ClO3��2 | CaCl2 | KClO3 | KCl |
| �ܽ��/g | 209.0 | 74.5 | 7.3 | 34.2 |
��2����Ӧ2Ϊ���ֽⷴӦ������ҺA�к��е�����ΪCaCl2��KClO3���ѧʽ��������Ϊ�÷�Ӧ�ܵõ�KClO3�����ԭ������ͬ�����£�����ص��ܽ����С��
��3��ϴ��KClO3����ʱ����ѡ������Cϴ�Ӽ�������ĸ��ţ���
A��KCl������Һ B����ˮ C������KClO3��Һ
���Ʊ���ϸCaCO3��������ͼ2��ʾ����֪��NH4Cl��Һ�����ԣ�
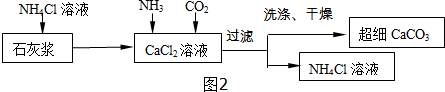
��1����CaCl2��Һ��ͨ���������壬���ɳ�ϸCaCO3�Ļ�ѧ����ʽCaCl2+H2O+CO2+2NH3�TCaCO3��+2NH4Cl�������̿�ѭ��ʹ�õ��������Ȼ����Һ��
��2������CaCO3�Ƿ�ϴ�Ӹɾ��ķ����ǣ�ȡ���һ��ϴ��Һ�������еμ�B����д��ţ����۲죬����ʵ�������ƶ��Ƿ�ϴ�ɾ���
A��Na2CO3��Һ B��AgNO3��Һ C����̪��Һ��
��֪������ڲ�ͬ�¶�����ˮ��Һ������Һ�е��ܽ�ȣ�g��
| �¶ȣ��棩 | 0 | 10 | 26 | 30 |
| ˮ��Һ | 7.31 | 9.28 | 11.03 | 12.98 |
| ����8%����Һ | 1.41 | 1.58 | 2.25 | 3.36 |
| ����35%����Һ | 0.44 | 0.75 | 0.82 | �dz�ѹ |
��2���������а�ˮŨ�ȳ���������25%��40%����ԭ���ǰ�ˮŨ��Խ��������ܽ��ԽС���������¶����˱���
���£�ѡ����¡����¡�����
��3����Һ���������������ѭ��ʹ�õ����壬�仯ѧʽΪNH3����Һ�еĸ���Ʒ�Ȼ��ƿ�ת����̼��ƹ��壬��HNO3��Ӧ�Ʊ�Ca��NO3��2•6H2O���壬Ϊȷ���Ʊ������мȲ�����ˮ��Ҳ�����ˮ������������Һ���������ܼ���������Ϊ7��5��
��4��ʵ���ҽ��й��˲�����Ҫ�IJ����������ձ�����������©�������в�������ϡ��Ũ����ʱҲ�õ���ϡ��Ũ����ʱ�õ�����������Ҫ����Ϊʹ�ܽ������������ʱɢ������ֹ�ֲ����ȶ�����Һ��ɽ���
��5����������Ƿ�ϴ�����Լ���AB������ţ�
A����̪��Һ B̼������Һ C�Ȼ�����Һ
��6��������������Ч���ٶ���������ŷţ��ܽ���ת��Ϊʯ�ࣨCaSO4•2H2O���Ȳ�Ʒ��ʵ�֡����Ϊ����������������ŷŻᵼ�µĻ����������γ����꣬���ø��������Һ���������ж�������
��7��ij�糧��ú200�֣�������������Ϊ2.5%������ȼ��ʱú�е���ȫ��ת���ɶ�������������������96%����ת��Ϊʯ�ࣨCaSO4•2H2O�����������ʯ����ٶ֣�
��1��̽��ϡ����������������Һ�ķ�Ӧ��
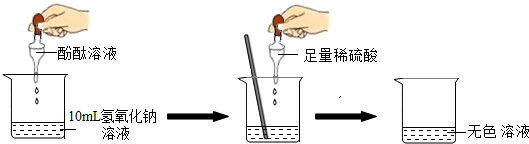
�����뼸�η�̪��Һ����Һ����ɫ��Ϊ��ɫ����������ʵ������ɫ�仯����ȷ��ϡ����������������Һ�����˻�ѧ�仯����Ӧ�Ļ�ѧ����ʽΪ��2NaOH+H2SO4=Na2SO4+2H2O��
��2��̽������ϡ����������������Һ��Ӧ���ձ��е������Ƿ������
����������Ӧ��������Һ�����ɫ������ȷ��ϡ�����Ƿ������ͬѧ���ֱַ�ѡȡ�Ȼ�����Һ����ɫʯ����Һ���ʵ�鷽���������жϲ�������
| ʵ�鷽�� | ʵ�鲽�� | ʵ������ | ʵ����� |
| ����һ | ȡ���������������Ȼ�����Һ | ���ְ�ɫ���� | ϡ������� |
| ������ | ȡ�������뼸����ɫʯ����Һ | ��Һ��� | ϡ������� |
����һ��ʵ�鷽�������ԭ����NaOH��H2SO4��Ӧ�����ɵ�������Ҳ�ܺ�BaCl2��Ӧ������ɫ����BaSO4��
�������һ��ȷ��ϡ�����Ƿ������ʵ�鷽������ѡ�õ�ҩƷ��п������̼���Ƶȣ���ʵ������������������ų���֤��ϡ�����������֮ϡ���������
С����ΪNaOH��Һ��H2SO4��Һ���ʱû�����Ե�������˵�������Ƿ����˷�Ӧ��
���������ͼʵ��֤������֮��ȷʵ�����˷�Ӧ�����õ��Լ���NaOH��Һ��H2SO4��Һ��CuSO4��Һ�����ڼ�ͷ�Ϸ��������������Լ����ƣ����á�������������������ָ���Լ���������
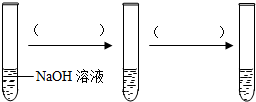
��2�������CuSO4��Һ������һ���Լ���ֻҪ���Լ��������ʵ����ܼ����Լ���˳����Σ�����֤�����߷����˷�Ӧ�������Լ��Ƿ�̪��Һ����ʯ����Һ����
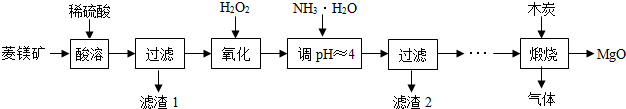
���ϣ��ٲ�ͬ�������������pH��Χ��
| �������� | Fe��OH��3 | Mg��OH��2 |
| ��ʼ������pH | 1.5 | 8.6 |
| ��ȫ������pH | 3.2 | 11.1 |
�۸��������Һֻ����SO2��������CO2��
�ܼ���Һ������SO2��������CO2��
�Իش��������⣺
��1��MgCO3��ϡ���ᷴӦ�Ļ�ѧ����ʽΪMgCO3+H2SO4=MgSO4+H2O+CO2����
��2������H2O2Ŀ���������������½�FeSO4������Fe2��SO4��3��ͬʱ����ˮ��������Ӧ�Ļ�ѧ����ʽΪ2FeSO4+H2SO4+H2O2=Fe2��SO4��3+2H2O��
��3���Ӱ�ˮ������Һ��pHԼΪ4��Ŀ���ǣ���Ӧ�Ļ�ѧ����ʽΪFe2��SO4��3+6NH3•H2O=3��NH4��2SO4+2Fe��OH��3�������˺���Һ�к����������ӣ�
��4�����չ��̴������·�Ӧ��
2MgSO4+C$\frac{\underline{\;800��\;}}{\;}$2MgO+2SO2��+CO2��
MgSO4+C$\frac{\underline{\;800��\;}}{\;}$MgO+SO2��+CO��
MgSO4+3C$\frac{\underline{\;800��\;}}{\;}$MgO+S��+3CO��
������ͼװ�ö����ղ�����������зֲ����ջ��ռ���������ÿ����Ӧ����ȫ���У�

��A�������ǣ������ܱڳ���ɫ���壻
��B��ʢ�ŵ���Һ������d������ĸ����ʵ������Ϊ��Һ��ɫ��
a��Ca��OH��2��Һ b��Na2CO3��Һ c��ϡ���� d��KMnO4��Һ
��C��ʢ�ŵ���Һ����������������Һ��������CO2���壬D���ռ���������CO���ѧʽ����
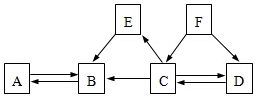 ���л�ѧ�м��ֳ�������֮����ת����ϵ��ͼ��ʾ����֪������B��CΪ���壬��B��ֲ����й�����õ�һ����Ҫԭ�ϣ�D��F��Ϊ��ɫҺ�壬����������ͬ��Ԫ����ɣ�E�Ǻ�ɫ���壬��ϡ���ᷴӦ�õ���ɫ��Һ�����ַ�Ӧ��������P��Ӧ��������ȥ����
���л�ѧ�м��ֳ�������֮����ת����ϵ��ͼ��ʾ����֪������B��CΪ���壬��B��ֲ����й�����õ�һ����Ҫԭ�ϣ�D��F��Ϊ��ɫҺ�壬����������ͬ��Ԫ����ɣ�E�Ǻ�ɫ���壬��ϡ���ᷴӦ�õ���ɫ��Һ�����ַ�Ӧ��������P��Ӧ��������ȥ����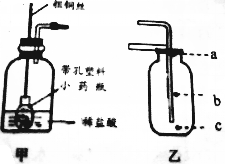 ����ͬѧ�ռ���һЩ��ͥװ��ʱ�����Ĵ���ʯ��Ƭ�����������ϵ�֪ͭ��ϡ���ᡢ�����Ӧ����˿������ϡ��������ᷴӦ���������������ͼ�ļס�����װ������ȡ������̼����ش��������⣺
����ͬѧ�ռ���һЩ��ͥװ��ʱ�����Ĵ���ʯ��Ƭ�����������ϵ�֪ͭ��ϡ���ᡢ�����Ӧ����˿������ϡ��������ᷴӦ���������������ͼ�ļס�����װ������ȡ������̼����ش��������⣺ ��ͼ��ʾ�DZ���֮Ϊ������ء���ֽ�ʵ�أ����ñ���ֽƬ��Ϊ�����壬����һ�߶�п������Ϊ��ظ�������һ�߶ƶ���������Ϊ�������������ܷ�ӦΪ��Zn+2MnO2+H2O=ZnO+2MnO��OH����
��ͼ��ʾ�DZ���֮Ϊ������ء���ֽ�ʵ�أ����ñ���ֽƬ��Ϊ�����壬����һ�߶�п������Ϊ��ظ�������һ�߶ƶ���������Ϊ�������������ܷ�ӦΪ��Zn+2MnO2+H2O=ZnO+2MnO��OH����