题目内容
5.将质量为44.4克含有少量NaCl的纯碱晶体(Na2CO3•nH2O)样品,平均分成A、B、C三份,进行如图实验(Na2CO3受热不分解).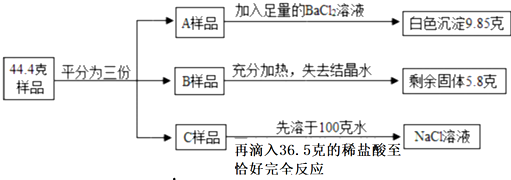
(1)A样品中与BaCl2溶液反应的Na2CO3的质量是5.3克.
(2)化学式Na2CO3•nH2O中n是10
(3)对C样品的操作结束后,所得NaCl溶液的溶质质量分数是多少?(精确到0.1%)
分析 碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)设碳酸钠质量为x,反应生成氯化钠质量为y,
BaCl2+Na2CO3═BaCO3↓+2NaCl,
106 197 117
x 9.85g y
$\frac{106}{x}$=$\frac{197}{9.85g}$=$\frac{117}{y}$,
x=5.3g,y=5.85g,
故填:5.3.
(2)结晶水的质量为:(44.4g÷3)-5.8g=9g,
根据题意有:$\frac{106}{5.3g}$=$\frac{18n}{9g}$,
n=10,
故填:10.
(3)设反应生成二氧化碳质量为z,
对C样品的操作结束后,所得NaCl溶液中的氯化钠质量为:5.8g-5.3g+5.85g=6.35g,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 44
5.3g z
$\frac{106}{5.3g}$=$\frac{44}{z}$,
z=2.2g,
反应所得溶液质量为:(44.4g÷3)+100g+36.5g-2.2g=149.1g,
所得NaCl溶液的溶质质量分数是:$\frac{6.35g}{149.1g}$×100%=4.3%,
答:所得NaCl溶液的溶质质量分数是4.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | Fe、Ag | B. | Fe、Zn | C. | Zn、Ag | D. | Zn、Ag、Fe |
| A. | 青蒿素属于有机物,由碳、氢、氧3个元素组成 | |
| B. | 青蒿素由15个碳原子、22个氢原子、5个氧原子构成 | |
| C. | 甲醇、乙醇在空气中充分燃烧一定都能生成二氧化碳和水 | |
| D. | 青蒿素中碳、氢、氧元素的质量比为15:22:5 |
| A. | CH4 | B. | NO2 | C. | N2O | D. | N2O4 |
| A. |  滴加液体 | B. |  稀释浓硫酸 | C. | 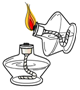 点燃酒精灯 | D. | 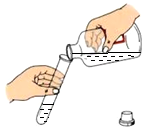 倾倒液体 |
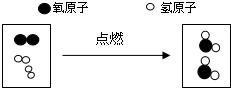 如图是某化学反应的微观示意图(表示氧原子,表示氢原子)
如图是某化学反应的微观示意图(表示氧原子,表示氢原子)