题目内容
油条是人们喜欢的早点,中国油条的传统加工配方是用明矾(KAl(SO4)2)作为膨松剂,明矾常引起铝残留影响人体健康问题,现在的膨松剂常用臭粉(碳酸氢铵)、小苏打.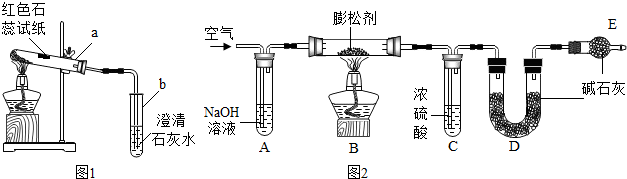
(1)油条中的主要营养素是油脂和
(2)“铝残留影响人体健康”中的铝是指 (选填“原子”或“元素”或“单质”)
(3)已知某膨松剂含碳酸氢铵、碳酸氢钠中的一种或两种,兴趣小组对该膨松剂进行如下探究:
【查阅资料】①2NaHCO3
Na2CO3+H2O+CO2↑; NH4HCO3
NH3↑+H2O+CO2↑.
②氨气能使湿润的红色石蕊试纸变蓝.浓硫酸可用于吸收氨气.
③碱石灰是固体氢氧化钠和氧化钙的混合物,能作干燥剂,和二氧化碳反应,不与氨气反应.
实验I:探究膨松剂的成分按图1所示连接好装置.
实验记录
【得出结论】:该膨松剂的成分为 (写出化学式).
实验Ⅱ:探究产生气体的量
①测定二氧化碳的质量:如图2所示装置(气密性良好,各装置中的试剂为足量).
将8g膨松剂装入装置B中,加热前,先对已连接好的装置A、B和C通一段时间的空气,再连接装置D、E;加热过程中,装置C的作用是 ;停止加热后,继续通入一段时间的空气,目的是 .实验中,测定实验前后装置 (填字母序号)的质量,其质量差即为样品产生的二氧化碳气体的质量.若没有装置A,可能会造成测定结果 (填“偏大”、“不变”或“偏小”).
②测定氨气的质量:将上图装置中 (填字母序号) 的连接顺序为对调.另取8g膨松剂装入装置B中,通过测定实验前后盛有浓硫酸的试管质量,其质量差即为样品产生的氨气的质量.若该装置的质量增加了1.36g,则同时共产生二氧化碳质量是多少?(有计算过程,结果精确到0.01)

(1)油条中的主要营养素是油脂和
(2)“铝残留影响人体健康”中的铝是指
(3)已知某膨松剂含碳酸氢铵、碳酸氢钠中的一种或两种,兴趣小组对该膨松剂进行如下探究:
【查阅资料】①2NaHCO3
| ||
| ||
②氨气能使湿润的红色石蕊试纸变蓝.浓硫酸可用于吸收氨气.
③碱石灰是固体氢氧化钠和氧化钙的混合物,能作干燥剂,和二氧化碳反应,不与氨气反应.
实验I:探究膨松剂的成分按图1所示连接好装置.
实验记录
| 实验操作 | 主要实验现象 | 实验结论 及解释 | |
| ① | 检查装置的气密性 | 装置的气密性良好 | |
| ② | 点燃酒精灯 | 试管中白色固体减少,红色石蕊试纸 | 有二氧化碳和氨气生成 |
| ③ | 继续充分加热 | 试管中仍有固体. | |
实验Ⅱ:探究产生气体的量
①测定二氧化碳的质量:如图2所示装置(气密性良好,各装置中的试剂为足量).
将8g膨松剂装入装置B中,加热前,先对已连接好的装置A、B和C通一段时间的空气,再连接装置D、E;加热过程中,装置C的作用是
②测定氨气的质量:将上图装置中
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,盐的化学性质,根据化学反应方程式的计算,生命活动与六大营养素
专题:科学探究
分析:(1)人类需要的营养物质有糖类、油脂、蛋白质、维生素、水和无机盐.
(2)物质中的中的“铝、铁、碘、氟”等不是以单质、分子、原子等形式存在,而是指元素.
(3)实验I:根据氨气的检验方法考虑;【得出结论】根据碳酸氢钠、碳酸氢铵加热的生成物考虑;
实验Ⅱ:①根据二氧化碳与氢氧化钠反应,浓硫酸可以吸收氨气和E装置的作用进行考虑;②根据浓硫酸质量的增加量考虑生成氨气的质量,在测量氨气质量之前需除去水蒸气和二氧化碳.根据氨气的质量,求碳酸氢铵及生成的二氧化碳质量,在用8g-碳酸氢铵质量=碳酸氢钠质量,求碳酸氢钠生成的二氧化碳质量,将二者质量相加.
(2)物质中的中的“铝、铁、碘、氟”等不是以单质、分子、原子等形式存在,而是指元素.
(3)实验I:根据氨气的检验方法考虑;【得出结论】根据碳酸氢钠、碳酸氢铵加热的生成物考虑;
实验Ⅱ:①根据二氧化碳与氢氧化钠反应,浓硫酸可以吸收氨气和E装置的作用进行考虑;②根据浓硫酸质量的增加量考虑生成氨气的质量,在测量氨气质量之前需除去水蒸气和二氧化碳.根据氨气的质量,求碳酸氢铵及生成的二氧化碳质量,在用8g-碳酸氢铵质量=碳酸氢钠质量,求碳酸氢钠生成的二氧化碳质量,将二者质量相加.
解答:解:(1)油条中的主要营养素是油脂和淀粉(糖类).
(2)“铝残留影响人体健康”中的“铝”不是以单质、分子、原子等形式存在,这里所指的“铝”是强调存在的元素,与具体形态无关.
(3)实验I:氨气能使湿润的红色石蕊试纸变蓝.
【得出结论】根据加热后有氨气生成,说明含有碳酸氢铵,充分加热后,玻璃管中仍有固体说明含有碳酸氢钠,碳酸氢钠加热后能生成碳酸钠固体;
实验Ⅱ:①C中浓硫酸具有吸水性,所以是为了除去气体中的水蒸气,硫酸能与氨气反应生成硫酸铵所以也除去了氨气;停止加热后,继续通入一段时间的空气,目的是将产生的二氧化碳全部排出,计算准确.碱石灰是固体氢氧化钠和氧化钙的混合物,能吸收二氧化碳,实验中,测定实验前后装置D的质量,其质量差即为样品产生的二氧化碳气体的质量.若没有装置A,造成空气中的二氧化碳被D吸收,会造成测定结果偏大.
②要测氨气的质量,先通入D中碱石灰,将水、二氧化碳除去,再通入C浓硫酸吸收氨气,C装置质量的增加量就是氨气的质量,装置E是防止空气中水分进入C装置;故连接顺序为A、B、D、C、E(或B、D、C、E)
解:设8g膨松剂中韩碳酸氢铵的质量为x,同时生成二氧化碳的质量为y
NH4HCO3
NH3↑+H2O+CO2↑.
79 17 44
x 1.36g y
=
x=6.32g
=
y=3.52g
所以碳酸氢钠的质量为8g-6.32g=1.68g
设碳酸氢钠生成的二氧化碳质量为z
2NaHCO3
Na2CO3+H2O+CO2↑;
168 44
1.68g z
=
z=0.44g
故共产生二氧化碳质量为3.52g+0.44g=3.96g.
故答案为:(1)糖类;(2)元素;(3)(实验I)变蓝;NaHCO3和 NH4HCO3(实验Ⅱ)①除去水蒸气和氨气;将产生的二氧化碳全部排出;D;偏大;②CD;3.96g
(2)“铝残留影响人体健康”中的“铝”不是以单质、分子、原子等形式存在,这里所指的“铝”是强调存在的元素,与具体形态无关.
(3)实验I:氨气能使湿润的红色石蕊试纸变蓝.
【得出结论】根据加热后有氨气生成,说明含有碳酸氢铵,充分加热后,玻璃管中仍有固体说明含有碳酸氢钠,碳酸氢钠加热后能生成碳酸钠固体;
实验Ⅱ:①C中浓硫酸具有吸水性,所以是为了除去气体中的水蒸气,硫酸能与氨气反应生成硫酸铵所以也除去了氨气;停止加热后,继续通入一段时间的空气,目的是将产生的二氧化碳全部排出,计算准确.碱石灰是固体氢氧化钠和氧化钙的混合物,能吸收二氧化碳,实验中,测定实验前后装置D的质量,其质量差即为样品产生的二氧化碳气体的质量.若没有装置A,造成空气中的二氧化碳被D吸收,会造成测定结果偏大.
②要测氨气的质量,先通入D中碱石灰,将水、二氧化碳除去,再通入C浓硫酸吸收氨气,C装置质量的增加量就是氨气的质量,装置E是防止空气中水分进入C装置;故连接顺序为A、B、D、C、E(或B、D、C、E)
解:设8g膨松剂中韩碳酸氢铵的质量为x,同时生成二氧化碳的质量为y
NH4HCO3
| ||
79 17 44
x 1.36g y
| 17 |
| 1.36g |
| 79 |
| x |
x=6.32g
| 17 |
| 1.36g |
| 44 |
| y |
y=3.52g
所以碳酸氢钠的质量为8g-6.32g=1.68g
设碳酸氢钠生成的二氧化碳质量为z
2NaHCO3
| ||
168 44
1.68g z
| 168 |
| 1.68g |
| 44 |
| z |
z=0.44g
故共产生二氧化碳质量为3.52g+0.44g=3.96g.
故答案为:(1)糖类;(2)元素;(3)(实验I)变蓝;NaHCO3和 NH4HCO3(实验Ⅱ)①除去水蒸气和氨气;将产生的二氧化碳全部排出;D;偏大;②CD;3.96g
点评:本题容易出错的地方是要知道硫酸可以吸收氨气,在验证氨气时要把水除掉,因为浓硫酸具有吸水性;在把装置B中的二氧化碳排到C装置时要注意空气中二氧化碳,必须先除去,才能再排气体.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某溶液pH=8,为使其pH降低为6应该( )
| A、滴加pH=3的硫酸 |
| B、滴加NaOH |
| C、加水 |
| D、倒出一半溶液 |
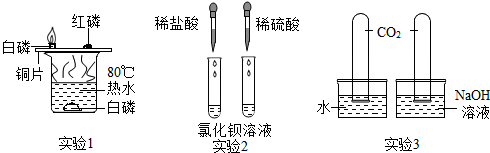
 根据金属活动顺序表的有关知识,回答下列问题:
根据金属活动顺序表的有关知识,回答下列问题:
