题目内容
12.元素周期表是我们学习和研究化学的重要工具.下表是元素周期表中1-18号元素原子核外电子排布,我对它进行研究:
(1)在Na H2O Na+ Ne F-中属于阳离子的是Na+,含10个质子和10个电子的是H2O、Ne.
(2)我发现如下规律:①原子序数与元素原子核电荷数在数值上相等;②同一行电子层数相同;③同一列最外层电子数相同.
(3)第17号元素的原子在化学反应中容易得(填“得”或“失”)电子,形成的离子符号为Cl-.
分析 (1)根据阳离子带正电荷和每个微粒中的质子数和电子数分析;
(2)根据提供的周期表,从横行和竖行来分析元素周期表中的规律;
(3)根据最外层电子数多于4个易的电子,少于4个易失去电子分析.
解答 解:(1)阳离子带正电荷,在Na、H2O、Na+、Ne、F-中属于阳离子的是Na+;氢是1号元素,一个氢原子里有一个质子、一个电子,氧是8号元素,一个氧原子里有8个质子、8个电子,氖是10号元素,一个氖原子里有10个质子、10个电子,因此H2O、Ne中含10个质子和10个电子.故答案为:Na+;H2O、Ne;
(2)根据周期表可以发现在同一周期的元素的原子结构中的电子层数都是相同的,如第二周期都是2个电子层,在同一竖行的最外层电子数都相同,如第一列,最外层电子数都是1,故答案为:同一行电子层数相同;同一列最外层电子数相同;
(3)从氯原子的原子结构示意图看,最外层电子数是7,所以易得一个电子,带一个单位负电荷,写在氯元素的右上角数字在前,正负号在后,由于数字是1要省略不写.故答案为:得; Cl-.
点评 本题考查元素原子的结构、最外层电子数的特点及与化学性质的关系和元素周期表的知识理解与应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.我们在实验室可以用加热高锰酸钾、加热氯酸钾和分解过氧化氢溶液的方法制取氧气,原因是这三种物质中均含有( )
| A. | 氧元素 | B. | 氧原子 | C. | 氧离子 | D. | 氧分子 |
17.化学学习可以帮助我们了解安全常识,你认为加油站内应该张贴的标志是( )
| A. |  当心爆炸 | B. |  严禁烟火 | C. |  节能标志 | D. |  绿色食品 |
4.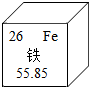 如图是元素周期表中铁的相关信息,结合所学内容,你认为下列有关铁的说法的中正确的是( )
如图是元素周期表中铁的相关信息,结合所学内容,你认为下列有关铁的说法的中正确的是( )
 如图是元素周期表中铁的相关信息,结合所学内容,你认为下列有关铁的说法的中正确的是( )
如图是元素周期表中铁的相关信息,结合所学内容,你认为下列有关铁的说法的中正确的是( )| A. | 铁是金属元素,原子序数为26,相对原子质量为58.85 | |
| B. | 生铁和钢是常见的铁合金,它们的性质和铁完全相同 | |
| C. | 铁在潮湿的空气中容易生锈,因此铁制品只能在真空中使用 | |
| D. | 铁由原子构成,常温下为固体,原子之间紧密排列,没有空隙 |
2.氧循环和碳循环密不可分,其中属于二氧化碳转化为氧气的变化是( )
| A. | 化石燃料的燃烧 | B. | 海水吸收二氧化碳 | ||
| C. | 动植物的呼吸作用 | D. | 绿色植物的光合作用 |
 如图所示,向小试管中加入一定量的下列物质,U形管液面右侧未发生改变,该物质是DF.
如图所示,向小试管中加入一定量的下列物质,U形管液面右侧未发生改变,该物质是DF.