题目内容
14.实验室有失去标签的四瓶无色溶液,分别为Ca(OH)2、Na2CO3、稀盐酸、NaCl溶液中的一种,为鉴别它们,现将这四瓶无色溶液分别标号为A、B、C、D,某校化学兴趣小组的同学邀你一同参与:【提出问题】A、B、C、D分别是什么溶液?
【实验药品】失去标签的四瓶溶液和无色酚酞试液.
【实验仪器】试管、胶头滴管、烧杯等.
【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| (1)分别取A、B、C、D溶液少量于试管中,两两混合 | A、B混合产生大量气泡,C、D混合无明显现象 | A、B是Na2CO3、稀盐酸溶液中的一种, C、D是Ca(OH)2、NaCl溶液中的一种 |
| (2)各取A、B、C、D溶液于四支试管中,分别滴加两滴无色酚酞试液,振荡 | A、D变红,B、C无明显现象 | A为Na2CO3溶液; C为NaCl溶液;由此区分出 B、D溶液 |
【继续探究】
将实验操作(2)实验后的四支试管中的溶液,倒入一洁净的烧杯中,充分反应静置后发现,烧杯底都有白色沉淀,上层清液为无色.则上层清液中一定含有的溶质是氯化钠(指示剂除外).可能含有的溶质是氯化钙.
分析 【收集证明】
根据四种物质间两两反应的现象进行推断,碳酸钠和盐酸能生成气体,碳酸钠和氢氧化钙反应有白色沉淀生成解答;
根据Ca(OH)2、Na2CO3溶液呈碱性,能使无色酚酞变红解答;
【反思与体会】碳酸钠和盐酸反应产生氯化钠、水和二氧化碳写出反应的方程式;
【继续探究】根据Na2CO3溶液加入Ca(OH)2溶液中生成碳酸钙沉淀和氢氧化钠.
解答 解:
【收集证明】
(1)分别取A、B、C、D溶液少量于试管中,两两混合,A、B混合产生大量气泡,碳酸钠和盐酸能生成气体,A、B是Na2CO3、稀盐酸溶液中的一种;
C、D混合无明显现象,Ca(OH)2和NaCl不反应,C、D是Ca(OH)2、NaCl溶液中的一种;
(2)各取A、B、C、D溶液于四支试管中,分别滴加两滴无色酚酞试液,振荡,A、D变红,B、C无明显现象,说明A是Na2CO3溶液,D是Ca(OH)2溶液
,C是NaCl溶液,B是稀盐酸;
【反思与体会】碳酸钠和盐酸反应产生氯化钠、水和二氧化碳,反应的方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【继续探究】
实验(2)后的四支试管中的溶液,倒入一洁净的烧杯中,充分反应静置后发现,烧杯底都有白色沉淀,盐酸先与氢氧化钙反应生成氯化钙和水,氯化钙再与碳酸钠反应生成碳酸钙沉淀和氯化钠,由于上层为无色透明的溶液,说明溶液不显碱性,所以不可能含有氢氧化钙,而氯化钙可能被碳酸钠反应掉,也可能没被反应掉.因此答案应该是:上层溶液中一定含有的溶质是NaCl(酸碱指示剂除外);可能含有的溶质是CaCl2;
故答案为:【进行实验】Na2CO3、稀盐酸; Ca(OH)2、NaCl; Na2CO3 NaCl;
【反思与体会】Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【继续探究】氯化钠;氯化钙.
点评 解答本题关键是要知道反应后溶液中溶质的判断方法是:先根据反应的生成物考虑,再考虑反应物是否过量.检验溶液是否含有氢氧化钠,可以用滴加无色酚酞试液进行检验.

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案| 试验次数 | 金属质量(g) | 金属氧化物质量(g) |
| 1 | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.0 |
| 平均值 | 45.0 | m |
(2)该金属氧化物中,R元素和氧元素的质量比为9:8;
(3)已知R的化合价为+3价,氧元素的相对原子质量为16,则R的相对原子质量为27.
| A. | +4 | B. | +2 | C. | +8 | D. | +2 |
| A. | 金属的锈蚀 | B. | 农家肥的腐熟 | C. | 植物的光合作用 | D. | 植物的呼吸作用 |
| A. | 燃烧常伴有发光、发热的现象,所以有发光、发热现象的一定是燃烧 | |
| B. | 点燃H2与O2混合气体可能爆炸,所以点燃CH4与O2的混合气体也可能爆炸 | |
| C. | 分解反应中都有多种物质生成,所以生成多种物质的反应一定是分解反应 | |
| D. | NaCl溶于水时,溶液温度无明显变化,所以NH4NO3溶于水时溶液温度也无明显变化 |
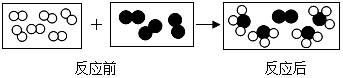 用“
用“ ”和“
”和“ ”分别代表氢气、氮气分子,它们在一定条件能发生化学反应,反应前后的模拟模型如图所示,下列说法中不正确的是( )
”分别代表氢气、氮气分子,它们在一定条件能发生化学反应,反应前后的模拟模型如图所示,下列说法中不正确的是( )| A. | 参加反应的“ ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| B. | 该反应是化合反应 | |
| C. | 该反应生成物的化学式为NH3 | |
| D. | 该反应说明化学反应实质是分子破裂、原子重新组合 |
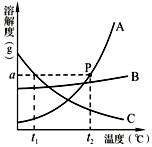 A、B、C三种物质的溶解度曲线如图所示.
A、B、C三种物质的溶解度曲线如图所示.