题目内容
 为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
(1)A点产生气体的质量为______;
(2)试样中碳酸钠的质量分数(结果精确到0.1%);
(3)A点时生成物溶液的溶质质量分数(结果精确到0.1%);
(4)B点时,烧杯内溶液中溶质的化学式______.
解:(1)A点产生气体的质量为:6g+36.5g-40.3g=2.2g;
(2)设6g试样中Na2CO3质量为x,生成氯化钠的质量是y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
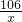 =
=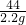 x=5.3g
x=5.3g
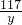 =
=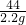 y=5.85g
y=5.85g
试样中Na2CO3的质量分数=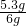 ×100%≈88.3%
×100%≈88.3%
(3)答:试样中Na2CO3的质量分数为88.3%.
(3)试液中氯化钠的质量是6g-5.3g=0.7g,所以A点时生成物溶液的溶质质量分数: ×100%≈16.3%;
×100%≈16.3%;
(4)当碳酸钠和盐酸恰好完全反应时,溶液中的溶质是氯化钠,但到B点时盐酸已过量,溶液中的溶质除了有氯化钠外还有盐酸中的溶质氯化氢;
故答案为:(1)2.2g;
(2)试样中Na2CO3的质量分数为88.3%;(3)A点时生成物溶液的溶质质量分数16.3%;(4)NaCl、HCl.
分析:(1)据图可知到A点时盐酸和碳酸钠恰好完全反应,生成气体的质量正好是烧杯中的物质前后减少的质量;
(2)利用碳酸钠与盐酸反应的化学方程式,根据二氧化碳的质量求出碳酸钠的质量,再根据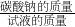 ×100%求出试样中碳酸钠的质量分数;
×100%求出试样中碳酸钠的质量分数;
(3)A点时盐酸和碳酸钠恰好完全反应,生成物溶液是氯化钠溶液,溶液中溶质既包括生成的氯化钠,还包括试液中的氯化钠,并据溶质的质量分数计算式计算此时溶液溶质的质量分数;
(4)到B点时,碳酸钠已反应完,还有剩余的盐酸,因而此时溶液中的溶质除了反应生成的溶质外还有剩余的盐酸中的溶质.
点评:本题主要考查了根据图象分析已知量并根据化学方程式进行相关方面计算,分析反应后溶液溶质质量分数时,要考虑试液中的杂质是否是溶质的一部分.
(2)设6g试样中Na2CO3质量为x,生成氯化钠的质量是y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
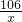 =
=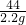 x=5.3g
x=5.3g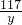 =
=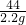 y=5.85g
y=5.85g试样中Na2CO3的质量分数=
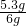 ×100%≈88.3%
×100%≈88.3%(3)答:试样中Na2CO3的质量分数为88.3%.
(3)试液中氯化钠的质量是6g-5.3g=0.7g,所以A点时生成物溶液的溶质质量分数:
 ×100%≈16.3%;
×100%≈16.3%;(4)当碳酸钠和盐酸恰好完全反应时,溶液中的溶质是氯化钠,但到B点时盐酸已过量,溶液中的溶质除了有氯化钠外还有盐酸中的溶质氯化氢;
故答案为:(1)2.2g;
(2)试样中Na2CO3的质量分数为88.3%;(3)A点时生成物溶液的溶质质量分数16.3%;(4)NaCl、HCl.
分析:(1)据图可知到A点时盐酸和碳酸钠恰好完全反应,生成气体的质量正好是烧杯中的物质前后减少的质量;
(2)利用碳酸钠与盐酸反应的化学方程式,根据二氧化碳的质量求出碳酸钠的质量,再根据
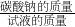 ×100%求出试样中碳酸钠的质量分数;
×100%求出试样中碳酸钠的质量分数;(3)A点时盐酸和碳酸钠恰好完全反应,生成物溶液是氯化钠溶液,溶液中溶质既包括生成的氯化钠,还包括试液中的氯化钠,并据溶质的质量分数计算式计算此时溶液溶质的质量分数;
(4)到B点时,碳酸钠已反应完,还有剩余的盐酸,因而此时溶液中的溶质除了反应生成的溶质外还有剩余的盐酸中的溶质.
点评:本题主要考查了根据图象分析已知量并根据化学方程式进行相关方面计算,分析反应后溶液溶质质量分数时,要考虑试液中的杂质是否是溶质的一部分.

练习册系列答案
相关题目
在研究酸和碱的化学性质时,某小组同学想证明:稀H2SO4与NaOH溶液混合后,虽然仍为无色溶夜,但确实发生了化学反应.请你与他们一起完成实验方案的设计、实施和评价.
(1)方案一:测定稀H2SO4与NaOH 溶夜混合前后的pH(20℃).测定某NaOH 溶夜的pH,pH______7(选填“大于”“等于”或“小于”).将一定量的稀H2SO4 加入该NaOH 溶夜中,混合均匀后测定其pH,pH小于7.
结论:稀H2SO4 与NaOH 溶液发生了化学反应,并且______过量.该反应化学方程式为______
(2)为了进一步获取稀H2SO4 与NaOH 溶液确实发生了化学反应的证据,依据中和反应是放热反应,H2SO4 与NaOH反应是______(选填“放热”“吸热”或“无热量变化”)的反应,采用稀H2SO4 与NaOH 溶液进行实验验证,具体操作是______.
(3)方案二:利用酸碱指示剂.回忆课堂上你和老师共同完成的酸、碱反应的实验探究,并依照下列要求进行实验的设计与分析:
①请你依据如图所示设计一个酸和碱反应的探究实验.

表1 探究实验
| 实验步骤 | 实验现象 | 结论 |
| a.向烧杯中加入10ml 氢氧化钠溶液,并滴入几滴酚酞溶液; b.再用滴管慢慢滴入稀硫酸,并不断搅拌 | a.溶液颜色______; b.不断搅拌溶液至溶液 颜色恰好变成______为止. | 酸和碱发生了中和反应, 该反应属四种基本反应 类型中的______反应. |
表2 探究实验
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
| 方案二 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好反应 |
| 方案三 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
某化学课外兴趣小组为探究Na与CO2的反应进行了如下实验(实验部分装置如右图所示):向盛有Na的装置A中通入纯净、干燥的CO2,当观察到装置B中刚好出现浑浊时,点燃酒精灯,同时继续缓缓通入CO2,Na剧烈燃烧,产生白烟,燃烧结束后装置A中有黑色固体和白色固体生成.

资料卡:
(1)K、Ca、Na等活泼金属的氧化物均可与水反应生成对应的碱;
(2)钠为银白色金属,过氧化钠为淡黄色固体.
(一)提出问题:白色固体含有什么物质?
(二)猜想与假设:
假设1:白色固体含有______;
假设2:白色固体含有Na2O;
(三)实验设计:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量白色固体放入足量水中 | 白色固体完全溶解 | |
| ②取①中少量溶液,加入______ | 产生大量气泡 | 假设1成立 |
| ③另取①中少量溶液,______ | ______ | 假设2成立 |
Na在CO2中燃烧存在多个反应、生成多种物质.请你写出其中生成物仅为一种白色固体与一种黑色固体的反应的化学方程式:______.
 完成下列变化的化学方程式,并注明反应类型.
完成下列变化的化学方程式,并注明反应类型.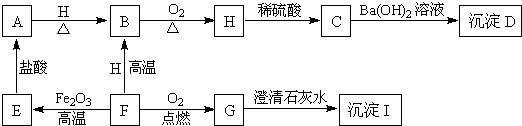
 Cu+CO2(置换反应)
Cu+CO2(置换反应)