题目内容
3.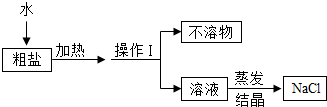 某化学活动小组对粗盐进行提纯,实验流程如图:
某化学活动小组对粗盐进行提纯,实验流程如图:(1)粗盐溶解过程中,加热的目的是加快粗盐的溶解速率.
(2)若食盐水中含有氯化钙,可用碳酸钠除去,请写出此反应的化学方程式:CaCl2+Na2CO3═CaCO3↓+2NaCl.
(3)操作Ⅰ的名称是过滤,用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(4)NaCl的用途很广,请列举氯化钠在生产、生活中的一种用途:配制生理盐水等.
分析 (1)根据温度升高,粒子运动的速率加快,进行分析解答.
(2)根据碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,写出反应的化学方程式即可.
(3)操作Ⅰ是将不溶物与溶液分离,进行分析解答.
(4)根据氯化钠的性质与用途,进行分析解答.
解答 解:(1)温度升高,粒子运动的速率加快,粗盐溶解过程中,加热的目的是加快粗盐的溶解速率.
(2)碳酸钠与氯化钙反应反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl.
(3)操作Ⅰ是将不溶物与溶液分离,操作Ⅰ的名称是过滤;用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(4)NaCl的用途很广,医疗上的生理盐水使用氯化钠配制的,农业上可以用氯化钠来选种,工业上可以用氯化钠为原料来制取碳酸钠、氢氧化钠、氯气和盐酸,生活中可以用氯化钠腌渍蔬菜、鱼、肉、蛋等.
故答案为:(1)加快粗盐的溶解速率;(2)CaCl2+Na2CO3═CaCO3↓+2NaCl;(3)过滤;漏斗;(4)配制生理盐水等.
点评 本题难度不大,掌握粗盐提纯的原理、盐的化学性质、过滤的原理与所需仪器、氯化钠的性质与用途等是正确解答本题的关键.

练习册系列答案
相关题目
14.在“蜡烛及其燃烧探究实验”中,属于化学变化的是( )
| A. | 燃烧中石蜡融化 | B. | 产物水蒸气凝结成小水珠 | ||
| C. | 蜡烛刚熄灭时产生白烟 | D. | 产物CO2使澄清石灰水变浑浊 |
15.下列图示的实验操作正确的是( )
| A. |  测溶液pH | B. | 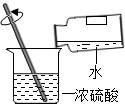 稀释浓硫酸 | ||
| C. | 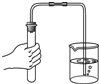 检查装置的气密性 | D. |  过滤 |
13.航天飞机表面覆盖石墨瓦可起到隔热和保护作用,这主要是利用石墨( )
| A. | 熔点高、化学性质稳定 | B. | 硬度小,有润滑作用 | ||
| C. | 密度小 | D. | 导电性 |