题目内容
4.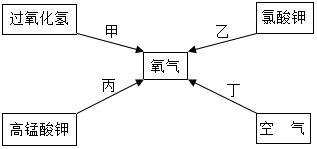 (1)这学期我们学习了多种制取氧气的方法,从元素利用率的角度考虑,你认为如图甲、乙、丙、丁四个途径中,氧元素利用率最高的化学途径是乙.
(1)这学期我们学习了多种制取氧气的方法,从元素利用率的角度考虑,你认为如图甲、乙、丙、丁四个途径中,氧元素利用率最高的化学途径是乙.(2)小明在实验时共收集了3瓶氧气,集气瓶的容积125毫升,已知氧气的密度为1.43克/升,请你帮小明计算:要完成实验,理论上至少需要加入5%的过氧化氢溶液多少克?
分析 过氧化氢在二氧化锰催化作用下分解生成水和氧气,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)过氧化氢在二氧化锰催化作用下分解生成水和氧气,氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,如图甲、乙、丙、丁四个途径中,氧元素利用率最高的化学途径是乙,这是因为乙中的氧元素完全转化成了氧气.
故填:乙.
(2)设理论上至少需要加入5%的过氧化氢溶液质量为x,
3瓶氧气质量为:1.43g/L×0.125L×3=0.54g,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x×5% 0.54g
$\frac{68}{x×5%}$=$\frac{32}{0.54g}$,
x=22.95g,
答:要完成实验,理论上至少需要加入5%的过氧化氢溶液22.95g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.下列有关溶液的说法正确的是( )
| A. | 具有均一性、稳定性的液体一定是溶液 | |
| B. | 配制溶液时,搅拌可以增强固体物质的溶解能力 | |
| C. | 饱和溶液的浓度一定比不饱和溶液的浓度大 | |
| D. | 融雪剂的原理是利用某些物质水溶液的凝固点低于0℃ |
9.中国科学家屠呦呦利用乙醚从黄花蒿汁液中提取抗疟特效药青蒿素,从而获得了2015年诺贝尔医学奖.已知青蒿素的化学式为C15H22O5,其分子中含有与H2O2类似的结构,下列叙述正确的是( )
| A. | 青蒿素属于氧化物 | B. | 1个青蒿素分子中含有11个氢分子 | ||
| C. | 青蒿素难溶于乙醚 | D. | 青蒿素的相对分子质量为282 |
 如图所示,是A、B、C三种固体物质的溶解度曲线,请据图回答下列问题:
如图所示,是A、B、C三种固体物质的溶解度曲线,请据图回答下列问题: