题目内容
2. 如图是硫酸试剂瓶标签上的内容.为了检验某钢材样品中铁的含量,需要把浓硫酸稀释为稀硫酸.根据计算回答下列问题:
如图是硫酸试剂瓶标签上的内容.为了检验某钢材样品中铁的含量,需要把浓硫酸稀释为稀硫酸.根据计算回答下列问题:(1)要将100g这种浓硫酸稀释为5%的稀硫酸,需要加水的质量是多少?
(2)将2g某钢铁样品加入足量稀释后的5%的稀硫酸中放出0.06g的气体,此钢铁样品中含铁的质量分数是多少?
分析 (1)根据?稀释前后,溶质质量不变进行分析;
(2)根据铁和稀硫酸反应生成硫酸亚铁和氢气,依据氢气的质量计算铁的质量,然后计算铁的质量分数.
解答 解:(1)需要加水的质量是:$\frac{100g×98%}{5%}$-100g=1860g;
(2)设参加反应的铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.06g
$\frac{56}{x}$=$\frac{2}{0.06g}$
x=1.68g
此钢铁样品中含铁的质量分数为:$\frac{1.68g}{2g}$×100%=84%.
故答案为:(1)需要水的质量为1860g;
(2)钢铁样品中含铁的质量分数为84%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
14.除去KCl溶液中混有的少量K2CO3,选用的试剂是( )
| A. | H2SO4溶液 | B. | 稀盐酸 | C. | NaCl溶液 | D. | AgNO3溶液 |
10.北京奥运会的火炬所用燃料是丙烷(C3H8),下列有关丙烷的说法不正确的是( )
| A. | 从组成上看:丙烷由碳、氢两种元素组成 | |
| B. | 从结构上看:一个丙烷分子由3个碳原子和8个氢原子构成 | |
| C. | 从性质上看:丙烷具有可燃性 | |
| D. | 从变化上看:丙烷完全燃烧只生成水 |
7.t℃时,在饱和硫酸铜溶液中加入少量白色硫酸铜粉末,溶液保持t℃,下列叙述正确的是( )
①有蓝色晶体析出
②饱和溶液总质量不变
③饱和溶液中溶质质量减少
④饱和溶液中溶剂质量减少
⑤饱和溶液的溶质质量分数减小
⑥饱和溶液的溶质质量分数不变.
①有蓝色晶体析出
②饱和溶液总质量不变
③饱和溶液中溶质质量减少
④饱和溶液中溶剂质量减少
⑤饱和溶液的溶质质量分数减小
⑥饱和溶液的溶质质量分数不变.
| A. | ①③④⑥ | B. | ①③④⑤ | C. | ①②⑥ | D. | ①⑤ |
12.某同学拟探究物质燃烧的条件,请协助完成下列表格.
问题讨论:
(1)白磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)进行实验①时,如果在酒精灯上加热时间较长,蘸水的棉花球也会燃烧起来,其原因是因为加热时间过长时,水分全部被蒸发,则温度会上升至棉花的着火点,棉花就燃烧起来.
(3)实验②中利用了铜片具有导热性.
(4)实验③中做两次实验的目的是通过对比实验或对照实验.
| 实验步骤 | 实验装置图 | 实验现象 | 结论 |
| 实验①用棉花分别蘸取酒精和水,放到酒精灯火焰上加热片刻.(图1所示). | 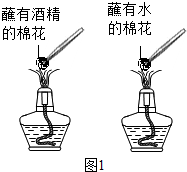 | 酒精燃烧,水没有燃烧 | 燃烧需要的条件之一是可燃物 |
| 实验②从乒乓球和滤纸上分别剪下同样大小的一小片,分别放在放在薄铜片的中部(图2所示). | 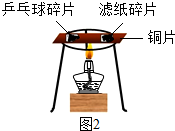 | 乒乓球片先燃烧,滤纸片后燃烧 | 燃烧需要的条件之一是温度达到着火点 |
| 实验③(1)将白磷放入8℃0热水中(图3所示). (2)将白磷放入80℃0热水中并通入氧气(图4所示). | 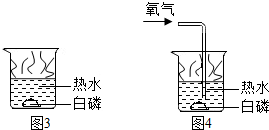 | 图3中的白磷不燃烧 图4中的白磷燃 烧 | 物质燃烧需要氧气 |
(1)白磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)进行实验①时,如果在酒精灯上加热时间较长,蘸水的棉花球也会燃烧起来,其原因是因为加热时间过长时,水分全部被蒸发,则温度会上升至棉花的着火点,棉花就燃烧起来.
(3)实验②中利用了铜片具有导热性.
(4)实验③中做两次实验的目的是通过对比实验或对照实验.