题目内容
13.为除去下列物质中的杂质(括号内为杂质),下列操作方法不能达到目的是( )| 选项 | 物质(杂质) | 操作方式 |
| A | Fe(Cu) | 加足量稀硫酸,充分反应后过滤 |
| B | NaOH溶液(Ca(OH)2) | 加入适量的Na2CO3,充分反应后过滤 |
| C | NaCl溶液(Na2CO3) | 加入过量盐酸 |
| D | Fe2(SO4)3溶液(CuSO4) | 加入足量铁屑,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Fe能与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、Ca(OH)2能与适量的Na2CO3反应生成碳酸钙白色沉淀和氢氧化钠,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、Na2CO3能与过量盐酸反应生成氯化钠、水和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、Fe2(SO4)3溶液和CuSO4均能与足量铁屑反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:AD.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
1.下列物质中,属于纯净物的是( )
| A. | 从空气中分离得到的稀有气体 | |
| B. | 经过沉淀、过滤得到的矿泉水 | |
| C. | 加热高锰酸钾完全反应后留下的固体 | |
| D. | 部分结冰的蒸馏水 |
18. CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
【查阅资料】
资料一:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列五种溶液的pH大小情况:
表中pH大小情况揭示出复分解反应的一条规律:较强酸发生类似反应可以生成较弱酸.下列反应中不符合该规律的是D(填字母)
A、H2SO4+Na2CO3=2NaCl+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
资料二:常见干燥剂有①五氧化二磷②无水氯化钙③碱石灰④生石灰⑤浓硫酸
【实验探究】
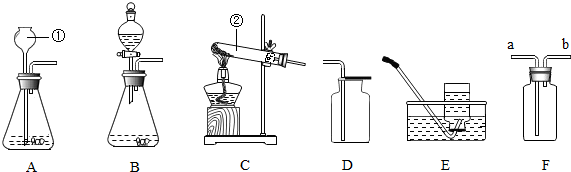
为了得到纯净的二氧化碳,设计了如图装置,请你分析:
a.制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
b.上述装置中,A是CuSO4溶液,B物质的名称可能是无水氯化钙(或五氧化二磷);
c.用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”).
 CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:【查阅资料】
资料一:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列五种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A、H2SO4+Na2CO3=2NaCl+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
资料二:常见干燥剂有①五氧化二磷②无水氯化钙③碱石灰④生石灰⑤浓硫酸
【实验探究】
为了得到纯净的二氧化碳,设计了如图装置,请你分析:
a.制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
b.上述装置中,A是CuSO4溶液,B物质的名称可能是无水氯化钙(或五氧化二磷);
c.用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”).
2.如图所示变化过程中发生物理变化的是( )
| A. |  蜡烛燃烧 | B. |  动植物的呼吸 | ||
| C. |  松花江水面结冰 | D. |  铜在潮湿的空气中生成铜绿 |
14.某化学兴趣小组的同学往氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象.
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
【评价反思】你认为实验设计方案不合理的同学是乙,理由是氢氧化钠固体溶于水也会放出热量.
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
| 同学 | 实验操作 | 现象 | 结论 |
| 甲 |  | 溶液由红色变成无色 | 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为HCl+NaOH=NaCl+H2O |
| 乙 | 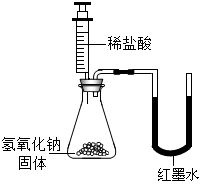 | U形玻璃管中左边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
| 丙 | 用pH试纸测定氢氧化钠溶液的pH;向其中滴加足量的稀盐酸后,再测定溶液的pH | 最后溶液的pH≤7(填“≥7”“≤7”或“不变”) | 氢氧化钠与盐酸发生了化学反应 |
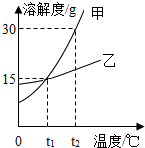 如图为甲、乙两物质的溶解度曲线.
如图为甲、乙两物质的溶解度曲线.