题目内容
16.将干冰放在空气中,其周围即刻产生大量的白雾,这是因为( )| A. | 干冰挥发出大量的水蒸气 | |
| B. | 干冰挥发出大量的白色二氧化碳气体 | |
| C. | 干冰被空气中的氧气氧化产生了大量的白色气体 | |
| D. | 干冰升华吸收了大量的热,使周围温度降低,大量的水蒸气凝结成了小液滴 |
分析 二氧化碳的用途有:①二氧化碳既不能燃烧也不能支持燃烧,因此二氧化碳能够灭火;②二氧化碳可以做化工原料,如制汽水等;③二氧化碳的固体干冰,可以进行人工降雨和制造云雾,也可以做制冷剂;④二氧化碳促进绿色植物的光合作用,因此可以做气体肥料.二氧化碳的固体干冰,可以进行人工降雨和制造云雾,也可以做制冷剂,因为干冰放到空气中,干冰升华时要吸收大量的热,其周围的温度迅速降低,使其周围产生大量的白雾,因而舞台上常用其制造云雾缭绕的幻境.
解答 解:二氧化碳的固体叫干冰,可以进行人工降雨和制造云雾,也可以做制冷剂,因为干冰放到空气中,干冰升华时要吸收大量的热,其周围的温度迅速降低,使其周围产生大量的白雾,因而舞台上常用其制造云雾缭绕的幻境;
故选D
点评 本考点考查了二氧化碳的固体干冰的用途,也充分体现了性质决定用途,用途又反映性质的理念.本考点基础性强,主要出现在选择题和实验题中.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
11. 实验室中有一瓶长期放置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
实验室中有一瓶长期放置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
[发现问题]该样品中含有哪些物质?
[查阅资料]①NaOH在空气中不会转化成NaHCO3.
②BaCl2溶液呈中性,Ba(OH)2是可溶性强碱.
③CO2在饱和的NaHCO3溶液中几乎不溶解.
[提出猜想]猜想Ⅰ:NaOH;
猜想Ⅱ:Na2CO3;
猜想Ⅲ:NaOH和Na2CO3.
[设计实验]
[收集证据]
(1)若现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅰ(填“猜想Ⅰ”、“猜想Ⅱ”或“猜想Ⅲ”)不成立.
(2)若X溶液为BaCl2溶液,现象A是有白色沉淀生成,则产生该沉淀的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl.取反应后的上层清液,测定其pH,当pH> 7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
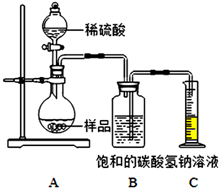
[定量分析]确定部分变质样品中Na2CO3的质量分数.兴趣小组的同学用如图所示装置进行实验.
步骤如下:
①按图连接好装置,并检查气密性;
②准确称取该样品1.0g,放入烧瓶内;
③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞.
④反应结束后,量筒内液体读数为55.0mL.
(已知:室温条件下,CO2的密度约为1.6g•L-1)
(1)B装置集气瓶内原有的空气对实验结果没有(填“有”或“没有”)影响.饱和碳酸氢钠溶液如果用水代替,则所测CO2的体积偏小(填“偏大”、“偏小”或“不变”),理由是二氧化碳会与水反应,易溶于水.
(2)计算该固体样品中Na2CO3的质量分数21.2%.(计算结果保留一位小数)
[实验反思]证明猜想Ⅲ是否成立,实验操作中的X溶液为BaCl2溶液,还可以改为滴加氯化钙溶液;取反应后的上层清液,除了测定其pH外,还可以滴加酚酞溶液.
 实验室中有一瓶长期放置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
实验室中有一瓶长期放置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.[发现问题]该样品中含有哪些物质?
[查阅资料]①NaOH在空气中不会转化成NaHCO3.
②BaCl2溶液呈中性,Ba(OH)2是可溶性强碱.
③CO2在饱和的NaHCO3溶液中几乎不溶解.
[提出猜想]猜想Ⅰ:NaOH;
猜想Ⅱ:Na2CO3;
猜想Ⅲ:NaOH和Na2CO3.
[设计实验]
| 实验操作 | 实验现象 |
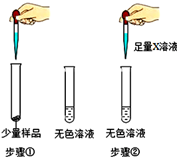 | 步骤①:样品全部溶解 步骤②:观察到现象A |
(1)若现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅰ(填“猜想Ⅰ”、“猜想Ⅱ”或“猜想Ⅲ”)不成立.
(2)若X溶液为BaCl2溶液,现象A是有白色沉淀生成,则产生该沉淀的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl.取反应后的上层清液,测定其pH,当pH> 7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
[定量分析]确定部分变质样品中Na2CO3的质量分数.兴趣小组的同学用如图所示装置进行实验.
步骤如下:
①按图连接好装置,并检查气密性;
②准确称取该样品1.0g,放入烧瓶内;
③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞.
④反应结束后,量筒内液体读数为55.0mL.
(已知:室温条件下,CO2的密度约为1.6g•L-1)
(1)B装置集气瓶内原有的空气对实验结果没有(填“有”或“没有”)影响.饱和碳酸氢钠溶液如果用水代替,则所测CO2的体积偏小(填“偏大”、“偏小”或“不变”),理由是二氧化碳会与水反应,易溶于水.
(2)计算该固体样品中Na2CO3的质量分数21.2%.(计算结果保留一位小数)
[实验反思]证明猜想Ⅲ是否成立,实验操作中的X溶液为BaCl2溶液,还可以改为滴加氯化钙溶液;取反应后的上层清液,除了测定其pH外,还可以滴加酚酞溶液.
8.节约用水和合理开发利用水资源是每个公民应尽的责任和义务,你认为下列做法与之无关的是( )
| A. | 洗菜、洗衣、淘米的水用来浇花、冲厕所 | |
| B. | 提倡使用节水器具 | |
| C. | 将活性炭放入硬水中使其软化 | |
| D. | 工业用水重复使用 |
6.请分析、比较以下几组化学反应,得出结论.
| 组别 | 化学方程式 | 结论 |
| Ⅰ | 6CO2+6H2O$\frac{\underline{\;光照叶绿素\;}}{\;}$C6H12O6+6O2 CO2+H2O═H2CO3 | 反应物相同,生成物不同,原因反应条件不同. |
| Ⅱ | Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | 反应物相同,生成物不同,原因反应物的浓度不同. |
| Ⅲ | C+O2(充足)$\frac{\underline{\;点燃\;}}{\;}$CO2 2C+O2(不充足)$\frac{\underline{\;点燃\;}}{\;}$2CO | 反应物相同,生成物不同,原因反应物的量不同. |
| Ⅳ | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑(反应缓慢) 2KClO3$\frac{\underline{\;二氧化锰\;}}{加热}$2KCl+3O2↑(反应迅速) | 反应物相同,生成物不同,原因有无催化剂. |
| 实践与应用 | 科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的“组合转化”技术,把过多二氧化碳转化为有益于人类的物质.若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: 2CO2+6H2$\frac{\underline{\;催化剂\;}}{△}$X+4H2O,推断X的化学式是C2H4. | |