题目内容
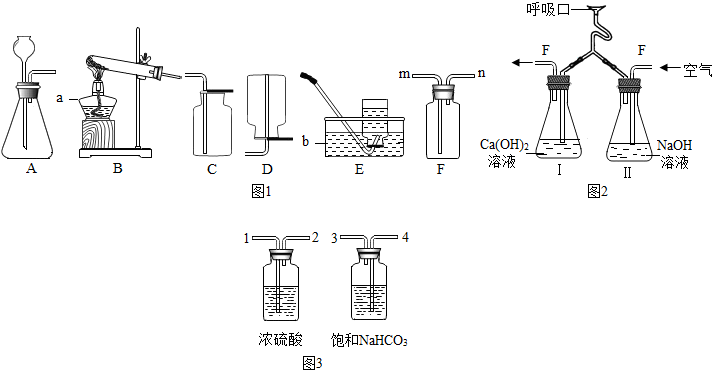
如图所示为实验室常见气体制备,净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器).某学校两个化学实验探究小组的同学欲用他们完成各自的探究实验.

(1)第一组的同学以锌粒和稀盐酸为原料,在实验室中制备、收集干燥纯净的氢气,按照要求设计实验装置、连接仪器,并检验装置的气密性.
①所选仪器的连接顺序为: (填写仪器序号字母).
②仪器A中所发生反应的化学方程式为: ;
③装置F的作用是 .
(2)第二组的同学以水煤气为原料(主要成分为CO,含有少量的水蒸气和CO2)来测定某氧化铜样品中 CuO 的质量分数(杂质不反应)取9g该样品,仪器的连接顺序为H1→B→G→H2→H3,试回答下列问题:
①实验时,观察到装置 G 中的现象为 .同学测得反应后G装置中固体的质量为7.4g,计算该样品中CuO的质量分数为 %(精确到 0.1%).若装置中没有连接仪器H1,利用装置H2反应前后的质量变化测算出样品中CuO的质量分数与实际值比较将会 .(填“偏小”“偏大”“基本一致”之一).
③该实验装置有一处明显不足,改进的方法是 .

(1)第一组的同学以锌粒和稀盐酸为原料,在实验室中制备、收集干燥纯净的氢气,按照要求设计实验装置、连接仪器,并检验装置的气密性.
①所选仪器的连接顺序为:
②仪器A中所发生反应的化学方程式为:
③装置F的作用是
(2)第二组的同学以水煤气为原料(主要成分为CO,含有少量的水蒸气和CO2)来测定某氧化铜样品中 CuO 的质量分数(杂质不反应)取9g该样品,仪器的连接顺序为H1→B→G→H2→H3,试回答下列问题:
①实验时,观察到装置 G 中的现象为
③该实验装置有一处明显不足,改进的方法是
考点:氢气的制取和检验,气体的干燥(除水),一氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:综合实验题,常见气体的实验室制法、检验、干燥与净化
分析:(1)通过A制取的氢气,可以通过F装置除去氯化氢气体,再通过B装置除去水蒸气,最后通过D装置可以收集到干燥纯净的氢气;
(2)氧化铜被还原成铜,G装置中固体减少的质量就是氧化铜中氧元素的质量,由此计算出氧化铜的质量,水煤气中含有二氧化碳,如果不除去,会导致计算出的氧化铜样品的纯度偏大;尾气中含有一氧化碳,有毒.
(2)氧化铜被还原成铜,G装置中固体减少的质量就是氧化铜中氧元素的质量,由此计算出氧化铜的质量,水煤气中含有二氧化碳,如果不除去,会导致计算出的氧化铜样品的纯度偏大;尾气中含有一氧化碳,有毒.
解答:解:(1)①通过A制取的氢气,可以通过F装置除去氯化氢气体,再通过B装置除去水蒸气,最后通过D装置可以收集到干燥纯净的氢气,所以连接顺序为:AFBD;
②锌粒和稀盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑;
③硝酸银溶液能够除去盐酸中挥发出来的氯化氢气体;
(2)①在加热的条件下,氧化铜与一氧化碳反应生成铜和二氧化碳,看到黑色粉末慢慢变成红色;
②G装置中固体的质量在反应后减少:9g-7.4g=1.6g,减少的质量即为氧化铜中氧元素的质量,则氧化铜的质量为:1.6g÷
×100%=8g;在样品中氧化铜的质量分数为:
×100%≈88.9%;仪器H1是用来除去水煤气中的二氧化碳,则装置H2中增重的质量比实际生成的二氧化碳的质量偏大,导致计算出样品中CuO的质量分数与实际值比较将会偏大;
③尾气中含有一氧化碳,一氧化碳有毒,不能直接排放到空气中,会污染空气,应该添加尾气收集装置.
故答案为:(1)①AFBD;②Zn+2HCl=ZnCl2+H2↑;③除去氢气中混有的氯化氢气体;
(2)①黑色粉末慢慢变成红色;②88.9;偏大;③将尾气点燃或收集.
②锌粒和稀盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑;
③硝酸银溶液能够除去盐酸中挥发出来的氯化氢气体;
(2)①在加热的条件下,氧化铜与一氧化碳反应生成铜和二氧化碳,看到黑色粉末慢慢变成红色;
②G装置中固体的质量在反应后减少:9g-7.4g=1.6g,减少的质量即为氧化铜中氧元素的质量,则氧化铜的质量为:1.6g÷
| 16 |
| 80 |
| 8g |
| 9g |
③尾气中含有一氧化碳,一氧化碳有毒,不能直接排放到空气中,会污染空气,应该添加尾气收集装置.
故答案为:(1)①AFBD;②Zn+2HCl=ZnCl2+H2↑;③除去氢气中混有的氯化氢气体;
(2)①黑色粉末慢慢变成红色;②88.9;偏大;③将尾气点燃或收集.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
下列各组括号内除杂质的方法或试剂错误的是( )
| A、铜粉中混有铁粉(用磁铁吸) |
| B、硝酸钠溶液中混有氯化钠(硝酸银溶液) |
| C、炭粉中混有氧化铜粉(稀硫酸) |
| D、氧化钙中混有碳酸钙(水、过滤) |
下列图标与燃烧和爆炸无关的是( )
A、 |
B、 |
C、 |
D、 |
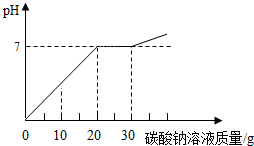 向21.88g含有少量氯化钙的稀盐酸中,逐滴滴加10.6%的碳酸钠溶液.所加入碳酸钠溶液的质量和溶液pH关系如图所示:
向21.88g含有少量氯化钙的稀盐酸中,逐滴滴加10.6%的碳酸钠溶液.所加入碳酸钠溶液的质量和溶液pH关系如图所示: