题目内容
非物质文化遗产“芜湖铁画”(镀金)含有金.铁(其他成分忽略不计).某同学取一定质量的铁画边角料,加入足量稀盐酸,充分反应后,放出0.3gH2,剩余固体质量为0.1g.
(1)求样品中铁的质量.
(2)求样品中金的质量分数.
考点:
根据化学反应方程式的计算.
专题:
有关化学方程式的计算.
分析:
因为金、铁这两种元素,只有铁可以和盐酸发生反应,产生氢气,故可根据化学方程式得出反应物之间的比例式,求出铁的质量;由题意可知,所以剩余固体就是金.
解答:
解:因为金、铁这两种元素,只有铁可以和盐酸发生反应,产生氢气,故可根据化学方程式得出反应物之间的比例式,求出铁的质量.剩余固体质量为0.1g即为金的质量.
解:设铁画边角料中所含铁的质量为x.
Fe+2HCl=FeCl2+H2↑
56 2
x 0.3g

x=8.4g
样品中金的质量分数= 100%≈1.1%
100%≈1.1%
答案:
(1)样品中铁的质量为8.4g
(2)样品中金的质量分数为1.1%
点评:
本题主要考查学生对铁生锈条件的认识,以及对物质质量分数的计算能力.学生必须熟知所给物质的性质,才能正确分析发生反应的过程,据此判计算物质质量,进而计算出质量分数.

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求:
(1)m的值为 g.
(2)12g石灰石样品中碳酸钙的质量等于 g.
(3)反应完全后最终溶液中氯化钙的质量分数? .
(写出计算过程,计算结果精确至0.1)
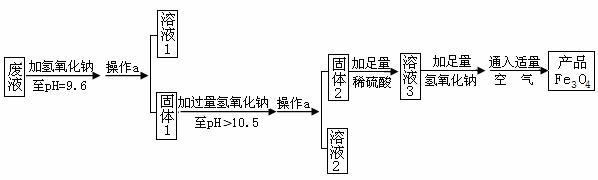 ZnSO4、MgSO4),进行四氧化三铁的制备流
ZnSO4、MgSO4),进行四氧化三铁的制备流 程如下:
程如下: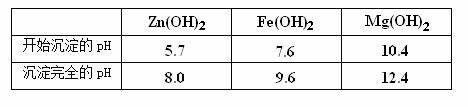
 生成沉淀的化学方程式为:
生成沉淀的化学方程式为:
 ,则需要改正的一点是_ __,请你写出用石灰石与稀盐酸反应制取二氧化
,则需要改正的一点是_ __,请你写出用石灰石与稀盐酸反应制取二氧化 碳的化学方程式_ __,将产生的二氧化碳气体通入澄清石灰水,可观察到的现象是_ __。
碳的化学方程式_ __,将产生的二氧化碳气体通入澄清石灰水,可观察到的现象是_ __。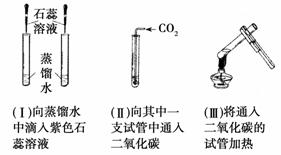

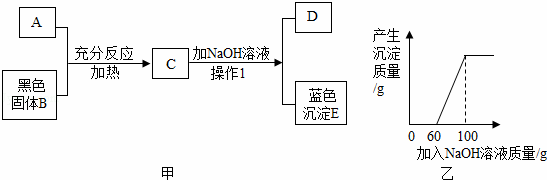
 能由NH4Cl、 Na2CO3 、NaCl 、NaOH 、Na2SO4中的一种或几种组成。为了确定其组成,某化学兴趣小组做了以下实验:
能由NH4Cl、 Na2CO3 、NaCl 、NaOH 、Na2SO4中的一种或几种组成。为了确定其组成,某化学兴趣小组做了以下实验:
 水+二氧化碳 B.磷+氧气
水+二氧化碳 B.磷+氧气