题目内容
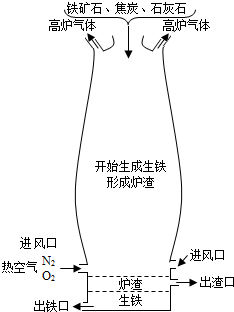 如图所示是高炉炼铁时高炉内的化学变化过程.认真阅读有关信息,回答下列问题:
如图所示是高炉炼铁时高炉内的化学变化过程.认真阅读有关信息,回答下列问题:(1)将铁从铁矿石中还原出来的物质是
(2)取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是
考点:铁的冶炼,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)在高炉中把铁还原出来的还原剂是一氧化碳.
(2)高炉炼出的铁是生铁,故加入盐酸会发生铁与盐酸的反应,观察并描述其反应现象,写出反应的化学方程式;此外还观察到不与盐酸反应的碳的出现,利用学过的相关的知识可解决此题.
(2)高炉炼出的铁是生铁,故加入盐酸会发生铁与盐酸的反应,观察并描述其反应现象,写出反应的化学方程式;此外还观察到不与盐酸反应的碳的出现,利用学过的相关的知识可解决此题.
解答:解:
(1)在高炉中是利用CO的还原性对氧化铁进行还原即可.故答案为:CO.
(2)高炉所炼的铁是生铁,如取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是:有气泡产生、溶液逐渐变为浅绿色;发生反应的化学方程式为:Fe+2HCl═FeCl2+H2↑,当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质是碳;因此一定有单质铁与杂质碳,相关的反应与此有关;要证明碳的存在一般是让其燃烧看是否生成二氧化碳.方法是:将黑色固体放在坩埚内加热至其燃烧,并在火焰上方罩一个杯壁沾有澄清石灰水的烧杯,杯壁出现白色斑点.
故答案为:
(1)CO
(2)有气泡产生,溶液逐渐变为浅绿色 2HCl+Fe=FeCl2+H2↑ C
将黑色固体放在坩埚内加热至其燃烧,并在火焰上方罩一个内壁沾有澄清石灰水的烧杯,烧杯内壁出现白色斑点
(1)在高炉中是利用CO的还原性对氧化铁进行还原即可.故答案为:CO.
(2)高炉所炼的铁是生铁,如取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是:有气泡产生、溶液逐渐变为浅绿色;发生反应的化学方程式为:Fe+2HCl═FeCl2+H2↑,当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质是碳;因此一定有单质铁与杂质碳,相关的反应与此有关;要证明碳的存在一般是让其燃烧看是否生成二氧化碳.方法是:将黑色固体放在坩埚内加热至其燃烧,并在火焰上方罩一个杯壁沾有澄清石灰水的烧杯,杯壁出现白色斑点.
故答案为:
(1)CO
(2)有气泡产生,溶液逐渐变为浅绿色 2HCl+Fe=FeCl2+H2↑ C
将黑色固体放在坩埚内加热至其燃烧,并在火焰上方罩一个内壁沾有澄清石灰水的烧杯,烧杯内壁出现白色斑点
点评:此题是对炼铁高炉知识的考查,解题的关键是了解炼铁高炉中发生的具体变化,属基础性知识考查题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在H2O、OH-、H、Cu四种微粒中,属于分子的是( )
| A、OH- |
| B、H |
| C、H2O |
| D、Cu |
下列物质能够反应,且反应类型是复分解的是( )
| A、Na2CO3溶液加入澄清石灰水中 |
| B、Fe2O3加入NaOH溶液中 |
| C、CO2通入澄清石灰水中 |
| D、稀HCl滴入NaOH溶液中 |
下列物质中,能与镁、氧化镁、氢氧化钠、硝酸银都反应的是( )
| A、氯化钡 | B、生石灰 |
| C、硝酸 | D、盐酸 |
下列物质由离子直接构成的是( )
| A、冰 | B、金刚石 | C、氯化钠 | D、氢气 |
 西瓜可清热解暑、除烦止渴,如图列出了西瓜的营养成分.
西瓜可清热解暑、除烦止渴,如图列出了西瓜的营养成分.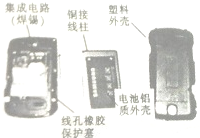 随着通信行业的迅速发展,在中国农村地区,固定电话的普及率已经降至46%,手机的普及率则上升至90%,手机为人类带来了更高效,更便利的生活,如图所示为手机的构造,回答下列问题:
随着通信行业的迅速发展,在中国农村地区,固定电话的普及率已经降至46%,手机的普及率则上升至90%,手机为人类带来了更高效,更便利的生活,如图所示为手机的构造,回答下列问题: