题目内容
2. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )
一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )| A. | 丁是该反应的催化剂 | B. | 参与反应的乙、丙质量比为3:17 | ||
| C. | 该反应的基本类型是分解反应 | D. | 参与反应的甲、丙质量比为7:10 |
分析 本题可分析甲~丁四种物质反应前后各物质的质量分数,确定是反应物还是生成物,据此结合题意进行分析判断即
解答 解:由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了70%-42%=28%,故甲是反应物;同理可以通过图示确定乙的质量分数减少了14%-8%=6%,故乙是反应物;丙的质量分数增加了40%-6%=34%,丙是生成物;丁的质量分数不变,可能作该反应的催化剂,也可能没有参加反应.
A、丁的质量分数不变,可能没有参加反应,也可能作该反应的催化剂,故选项说法错误;
B、该反应中乙、丙的质量比为6%:34%=3:17,故选项说法正确;
C、该反应的反应物为甲和乙,生成物是丙,符合“多变一”的特征,属于化合反应,故选项说法错误;
D、该反应中甲、丙的质量比为28%:34%=14:17,故D选项说法错误.
故选B.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析图中数据,灵活运用质量守恒定律.

练习册系列答案
相关题目
13.下表为各物质所含的少量杂质以及除去这些杂质应选用的试剂或操作方法.正确的一组为( )
| 序号 | 物 质 | 杂 质 | 除杂质应选用的试剂或操作方法 |
| ① | Cu | Fe | 加入足量稀盐酸,充分反应后,过滤、洗涤、干燥 |
| ② | 氮气 | 氧气 | 通过足量的灼热的铜网 |
| ③ | CO2 | HCl、H2O | 依次通过盛有足量饱和NaHCO3溶液和浓硫酸的洗气瓶 |
| ④ | NaCl溶液 | CaCl2、MgCl2、Na2SO4 | 依次加入过量的BaCl2溶液、Na2CO3溶液、NaOH溶液,充分反应后过滤,再滴加稀盐酸调节溶液pH为7 |
| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ①②④ |
10.小明和几位同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.他们马上停止实验,对这时烧杯内溶液中的溶质的成分展开了辩论.
(1)他们依据所学的化学知识,对烧杯内溶液中的溶质的成分作了如下猜想:
①可能是CaCl2; ②CaCl2与和Ca(OH)2; ③可能是CaCl2与和HCl组成的混合溶液
小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液.振荡.观察到酚酞试液不变色.于是他排除了猜想②,
小花想用碳酸钠溶液来验证剩下的两种猜想,请你帮她完成实验,填写以下表格:
(3)【拓展与应用】通过以上探究,最后发现猜想③正确.你认为上述烧杯内溶液如果未经处理直接倒入铁制下水道,可能造成的危害是腐蚀下水道.
(1)他们依据所学的化学知识,对烧杯内溶液中的溶质的成分作了如下猜想:
①可能是CaCl2; ②CaCl2与和Ca(OH)2; ③可能是CaCl2与和HCl组成的混合溶液
小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液.振荡.观察到酚酞试液不变色.于是他排除了猜想②,
小花想用碳酸钠溶液来验证剩下的两种猜想,请你帮她完成实验,填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液. | 猜想①正确 | |
| 猜想③正确 |
7.一定温度下,将溶液用水稀释,一定不变化的量是( )
| A. | 溶液的质量 | B. | 溶质的质量 | C. | 溶剂的质量 | D. | 溶质的质量分数 |
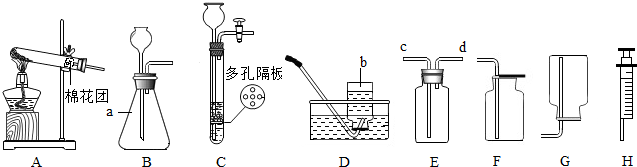
11.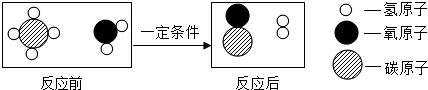 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )
甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )
 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )
甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )| A. | 该反应属于置换反应 | |
| B. | 水煤气的成分是一氧化碳和氧气 | |
| C. | 该反应中含氢元素的化合物有3种 | |
| D. | 该反应的化学方程式中甲烷和水的计量数之比为1:1 |
18.2014年6月,郑州市出台了“史上最严”的《建筑垃圾综合治理工作专项方案》,政府各部门努力协调、建立建筑垃圾资源化处理利用机制,为建筑垃圾“重生”寻找出路.建筑垃圾中废塑料、废橡胶制品属于( )
| A. | 金属材料 | B. | 有机合成材料 | C. | 无机非金属材料 | D. | 复合材料 |