题目内容
15.二氧化铂(PtO2)是一种催化剂.二氧化铂中铂元素的化合价是( )| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
分析 根据在化合物中正负化合价代数和为零,结合二氧化铂(PtO2)的化学式进行解答本题.
解答 解:氧元素显-2价,设铂元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
故选C.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.

练习册系列答案
相关题目
5.如表是所列是两种元素的部分信息,请用化学用语将表格补充完整:
| 元素符号 | 离子结构示意图 | 离子符号 | 它们组成的单质相互反应的化学方程式 |
| Al | 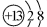 | Al3+ | 4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3 |
| O |  | O2- |
10.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A. | 硝酸钾 | B. | 橄榄油 | C. | 面粉 | D. | 泥土 |
20.如图为某化学反应的微观示意图,其中相同的球代表同种原子.下列说法正确的是( )


| A. | 反应前后原子种类改变 | B. | 反应前后分子个数不变 | ||
| C. | 反应前后元素种类不变 | D. | 分子在化学变化中不可分 |
17.用三块相同的铝片(均已去除氧化膜)进行如下实验.
实验①:取第一块铝片,放入稀硫酸中,有明显的现象;
实验②:取第二块铝片,放入CuSO4溶液中,铝片表面有红色物质析出;
实验③:取第三块铝片,放入浓硫酸中,竟然没有明显的现象;
实验④:将实验③中的铝片取出,洗净后放入CuSO4溶液中,也没有明显现象.
下列说法不正确的是( )
实验①:取第一块铝片,放入稀硫酸中,有明显的现象;
实验②:取第二块铝片,放入CuSO4溶液中,铝片表面有红色物质析出;
实验③:取第三块铝片,放入浓硫酸中,竟然没有明显的现象;
实验④:将实验③中的铝片取出,洗净后放入CuSO4溶液中,也没有明显现象.
下列说法不正确的是( )
| A. | 铝片与浓硫酸不能发生化学反应 | B. | 实验①观察到铝片表面有气泡产生 | ||
| C. | 由实验②可以得出金属铝比铜活泼 | D. | 浓硫酸与稀硫酸的化学性质有差别 |
 人体缺少钙元素会影响健康,因此每日需摄入足够的钙.某补钙剂说明书的部分内容如图所示,请完成下列问题.
人体缺少钙元素会影响健康,因此每日需摄入足够的钙.某补钙剂说明书的部分内容如图所示,请完成下列问题.
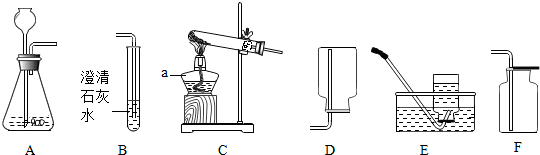
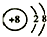 表示的粒子符号O2-.
表示的粒子符号O2-.