题目内容
12.已知一个碳12原子的质量为m千克,又知某种A原子中有a个质子,一个A原子的质量为n千克,则这种A原子的中子数为$\frac{12n-ma}{m}$.分析 根据某原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,相对原子质量=质子数+中子数,结合题意进行分析解答即可.
解答 解:已知一个碳12原子的质量为m千克,一个A原子的质量为n千克,则A原子的相对原子质量为$\frac{nkg}{mkg×\frac{1}{12}}$=$\frac{12n}{m}$;相对原子质量=质子数+中子数,由题意,A原子中有a个质子,则这种A原子的中子数为$\frac{12n}{m}$-a=$\frac{12n-ma}{m}$.
故答案为:$\frac{12n-ma}{m}$.
点评 本题难度不大,掌握原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$、相对原子质量=质子数+中子数并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
7.下列化合物中,氯元素为+1价的是( )
| A. | KClO3 | B. | PCl5 | C. | CuCl2 | D. | HClO |
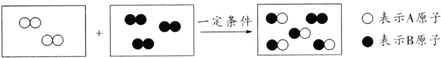
17.已知某反应前后分子变化的微观示意图如下图所示.下列说法错误的是( )

| A. | 点燃前,要先检验物质A的纯度,防止爆炸 | |
| B. | 物质B为单质,物质C、D为氧化物 | |
| C. | 该反应的基本反应类型为分解反应 | |
| D. | 该反应的化学方程式为:CH4+2O2$\underline{\underline{点燃}}$CO2+2H2O |
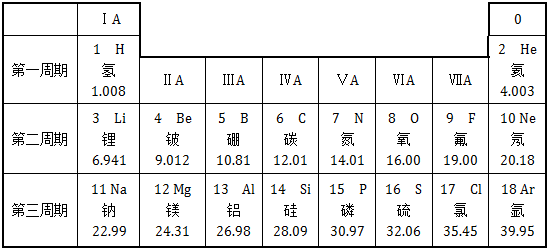
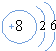 ,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是核电荷数不同.
,该微粒是元素周期表中的氧元素,它的核电荷数是8,碳元素的核电荷数是6,由此可知不同元素的本质区别是核电荷数不同.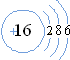 ,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.则硫形成的离子符号为S2-
,在化学反应中易得(填“得”或“失”)电子,是非金属(填“金属”或“非金属”)元素.则硫形成的离子符号为S2-
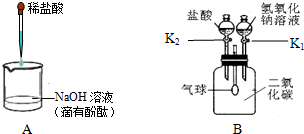
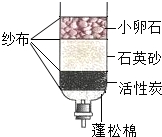 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.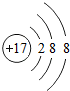 .
.