题目内容
7. 甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:(1)甲、丙两实验集气瓶中均放少量水,甲中加入少量水的目的是,甲瓶中反应的文字表达式为硫+氧气$\stackrel{点燃}{→}$二氧化硫.
(2)小明做完上述实验后,在乙中加入了一种无色液体,他所加的液体可能是澄清的石灰水(填名称),加该液体的目的是检验生成物是二氧化碳.
(3)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.他将镁条和不同含碳量的铁丝(铁丝直径均为0.4mm)放入氧气中燃烧,并将现象记录在下表中:
| 物质 | 镁 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,火星四射 |
②造成铁丝在氧气中燃烧时火星四射的主要原因是铁丝中含碳.
③铁丝在氧气中燃烧的文字表达式铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
分析 (1)硫燃烧时生成物会污染空气;
(2)考虑二氧化碳的检验即可.
(3)由实验数据分析,铁丝在氧气中燃烧产生火星的多少与含碳量有关.
解答 解:(1)由于硫和氧气反应生成的二氧化硫是对大气有污染的气体.所以,先在集气瓶中加入少量水的目的是吸收二氧化硫,防止对大气的污染;铁丝燃烧时在集气瓶底部放少量的水的目的是防止高温生成物溅落下来,炸裂瓶底.
(2)由于木炭与氧气反应生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊,常用澄清的石灰水来检验二氧化碳气体,所以,他所加的液体可能是澄清的石灰水,加该液体的目的是检验二氧化碳气体;
(3)由实验数据分析,铁丝在氧气中燃烧产生火星的多少与含碳量有关,通过对比可知铁丝含碳量越高,火星越多,所以铁丝在氧气中燃烧产生火星四射现象的原因,可能与铁丝中含碳有关.
故答案为:(1)吸收生成的二氧化硫,防止污染空气;硫+氧气$\stackrel{点燃}{→}$二氧化硫;
(2)澄清的石灰水;检验生成物是二氧化碳;
(3)①增大其与氧气的接触面积,尽快提高铁丝局部的温度;②铁丝中含碳;③铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
点评 本题难度不大,考查了氧气的化学性质,通过探究铁丝燃烧的实验,锻炼了学生分析问题、解决问题的能力.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
18.下列物质的用途,主要利用物理性质的是( )
| A. | 氢气做清洁高效的新能源 | B. | 氮气用作保护气 | ||
| C. | 金刚石用作玻璃刀 | D. | 小苏打焙制糕点的发酵剂 |
2.下列操作正确的是( )
| A. |  液体读数 | B. |  检查气密性 | C. |  点燃酒精灯 | D. |  加热液体 |
 用来测定空气成分的方法很多,如图所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:
用来测定空气成分的方法很多,如图所示的是小明用红磷在空气中燃烧的测定方法.实验过程是:
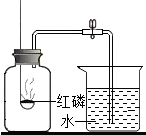 为测定空气里氧气的含量,甲、乙两位同学用如图所示装置进行了实验探究.
为测定空气里氧气的含量,甲、乙两位同学用如图所示装置进行了实验探究.