题目内容
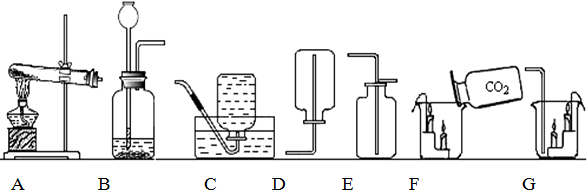
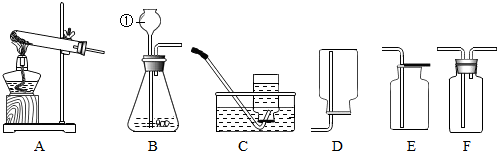
15.结合如图所示的实验装置,回答有关问题: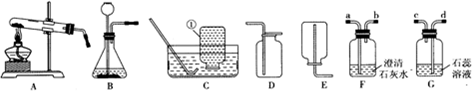
(1)仪器①的名称是集气瓶;
(2)在实验室里,常用大理石或石灰石跟稀盐酸反应制取二氧化碳.
①写出有关反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
②要制取4.4g二氧化碳完成性质实验,至少需要14.6%的盐酸的质量为50g;
③要证明二氧化碳能与水反应、能与澄清石灰水反应,将纯净干燥的CO2通过装置F、装置G时接口的连接顺序是dcab(用导管口的接口字母表示)
(3)氨气(NH3)是一种密度比空气小,极易溶于水的气体;在实验室里,常用加热氯化铵(NH4Cl)跟氢氧化钙固体混合物的方法来制取氨气,选择上述装置中的AE组合即可制取氨气.
分析 (1)熟练掌握常见的化学仪器名称和用途;
(2)①二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;
②根据二氧化碳的质量结合化学方程式即可计算出二氧化碳的质量;
③据二氧化碳与水反应生成碳酸,显酸性;二氧化碳能使澄清的石灰水变浑浊;
(3)发生装置的选择要根据反应物的状态和反应条件,收集装置要根据气体的密度和溶水性.
解答 解:(1)①为集气瓶;
(2)①二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;
②设若要生成4.4gCO2,参加反应的14.6%的盐酸质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
14.6%x 4.4g
则$\frac{73}{44}$=$\frac{14.6%x}{4.4g}$,解得x=50g;
③二氧化碳与水反应生成碳酸使紫色的石蕊试液变成红色,证明二氧化碳能与澄清石灰水反应,二氧化碳都应该从长管(b)进入,以便充分反应,现象明显,否则有可能会把液体压出装置.顺序为:dcab;
(3)氨气(NH3)是一种密度比空气小,极易溶于水的气体;在实验室里,常用加热氯化铵(NH4Cl)跟氢氧化钙固体混合物的方法来制取氨气,发生装置选择A,收集装置选择E.
故答案为:(1)集气瓶;(2)①CaCO3+2HCl=CaCl2+CO2↑+H2O; ②50; ③dcab;
(3)AE.
点评 本题考查了气体的制取和性质检验,属于基础性的考查,要求学生平时扎实基础,灵活运用.

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 用氢氧化钠溶液去除氧气中少量水蒸气 | |
| C. | 熟石灰能与稀盐酸反应,因此熟石灰用于治疗胃酸过多 | |
| D. | 鉴别羊毛与合成纤维,在空气中点燃,闻产生的气味 |
| A. | 验证碱能与酸反应:将H2SO4溶液滴入Cu(OH)2中 | |
| B. | 检验碳酸根离子:将要检验的物质与稀盐酸混合,观察是否产生气泡 | |
| C. | 验证质量守恒定律:将锌粒与稀硫酸混合,比较混合前后溶液的质量 | |
| D. | 鉴别H2、CH4、CO三种气体:分别将燃着的木条伸入集气瓶内,观察现象 |
| A. | 水 | B. | 金刚石 | C. | 硫酸铜 | D. | 氮气 |
| A. | 食醋 石油 | B. | 干冰 洁净的空气 | ||
| C. | 铜绿 海水 | D. | 五氧化二磷 酒精 |