题目内容
2.如图所示为实验室中常见的气体的制备、干燥、收集和性质实验的部分仪器,某校化学兴趣小组的同学欲用他们完成如下探究实验.试根据题目要求回答下列问题: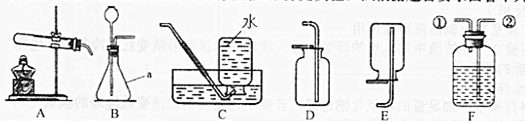
(1)标号a的仪器名称:锥形瓶
(2)小明同学以过氧化氢溶液为原料(MnO2为催化剂),在实验室中制备并收集一瓶干燥的氧气.若用F装置干燥,F中的干燥剂为浓硫酸,氧气从F装置哪端导管进入②(填序号);若用装置A制取氧气,其中所发生反应的化学方程为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)常温下铜与稀硫酸不反应,但铜与浓硫酸在加热时可以发生下列反应:
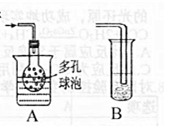
Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO+2H2O,SO2是一种有毒的气体,不能随意的排放到空气中,要用碱性(填酸性或碱性)溶液吸收.若要吸收更加充分,装置应该选择哪种?A(填A或B)
分析 (1)根据常用仪器的名称分析解答;
(2)根据浓硫酸具有吸水性可干燥氧气进行分析;根据装置的特点来确定制取氧气的药品和制取原理写出方程式;
(3)根据酸碱中和反应及吸收装置特点分析解答.
解答 解:(1)标号a的仪器名称是锥形瓶;
故答案为:锥形瓶;
(2)浓硫酸具有吸水性可干燥氧气,若用 F 装置干燥,且导管要长进短出,故导管要从②端进入,让气体与浓硫酸充分接触,然后从①端排出;装置A适用于固体加热制取氧气,实验室常用加热高锰酸钾或氯酸钾制氧气,因为装置A的试管口没有棉花,所以是用氯酸钾制取氧气,氯酸钾在二氧化锰的催化作用下受热分解为氯化钾和氧气,发生反应的化学方程为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
故答案为:浓硫酸;②;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)SO2是一种有毒的气体,不能随意排放到空气中,二氧化硫为酸性氧化物,可与碱性溶液反应,故要用碱性溶液吸收,吸收装置应该选择A,多孔球泡可让气体充分与氢氧化钠溶液接触,吸收更充分,且能有效防止液体倒吸.
故答案为:碱性;A.
点评 本考点主要考查了常用仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
5.现在正是人们赏春的好季节.一位游客在桃林不慎被蜜蜂蜇伤,为减轻酸性物质引起的痛痒,你建议该游客应在蜇伤处涂抹( )
| A. | 牛奶(pH≈6) | B. | 苹果汁(pH≈3) | C. | 牙膏(pH≈9) | D. | 矿泉水(pH≈7) |
6.下列符号:2N、N2、H2O、2CO、SO2 中,数字“2”的意义能用来表示分子个数的有( )
| A. | 2个 | B. | 1个 | C. | 4个 | D. | 5个 |
14.根据如图所示实验,下列对应的实验结果描述正确的是( )
| A. | 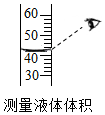 甲读数偏小 甲读数偏小 | B. | 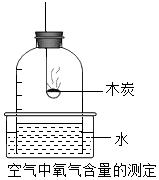 乙测量结果偏大 乙测量结果偏大 | ||
| C. | 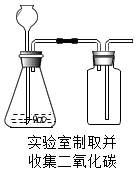 丙易收集满CO2 丙易收集满CO2 | D. | 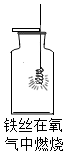 丁集气瓶易破裂 丁集气瓶易破裂 |
11.为达到实验目的,下列实验方案或结论不正确的是( )
| 实验目的 | 实验方案或结论 | |
| A | 鉴别NaCl溶液、Na2SO4溶液和(NH4)2SO4溶液 | 各取少量于试管中,分别滴加Ba(OH)2溶液,观察现象 |
| B | 除去铜粉中含有的少量铁粉 | 将混合固体加入到足量稀盐酸中,充分反应后过滤、洗涤、干燥 |
| C | 鉴别①CuSO4溶液;②稀H2SO4;③NaCl溶液;④NaOH溶液. | 不用其他任何试剂就能鉴别,且鉴别的顺序为①④②③或①④③② |
| D | 除去CO2中的少量HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |